| Специалистам > Лечение и реабилитация > Лечебная
физкультура
Белова А.Н.
Нейрореабилитация: Руководство для врачей
Москва, 2000.
Глава 9. Позвоночно-спинномозговая травма
Под позвоночно-спинномозговой травмой (ПСМТ) понимают механическое повреждение
позвоночника и/или содержимого позвоночного канала (спинного мозга, его оболочек
и сосудов, спинномозговых нервов). Частота ПСМТ в различных географических регионах
варьирует от 29.4 до 50 случаев на один миллион жителей, при этом более половина
пострадавших - лица моложе 40 лет; мужчины в сравнении с женщинами травмируются
в 2.5-4 раза чаще [Fine Р.R. и соавт., 1982; Yarkony G., Chen D., 1996].
Больные с позвоночно-спинномозговой травмой представляют собой наиболее тяжелый контингент реабилитационных
учреждений. Восстановительное лечение этих больных требует от медперсонала особого
терпения и мастерства. С 1940-х годов вначале в США и Великобритании, а затем
и во многих других странах для больных позвоночно-спинномозговой травмой стали создаваться специальные реабилитационные
центры. Своевременно оказанная квалифицированная реабилитационная помощь существенно
улучшает исходы травмы и повышает качество жизни пострадавшего [Bedbrook G.,1979].
9.1. ФАКТОРЫ, ОПРЕДЕЛЯЮЩИЕ НАПРАВЛЕННОСТЬ РЕАБИЛИТАЦИОННЫХ
МЕРОПРИЯТИЙ
Направленность реабилитационных мероприятий при позвоночно-спинномозговой травме зависит от множества факторов,
к основным из которых относятся следующие: тип и характер ПСМТ; стабильность
повреждения позвоночника; вид, уровень и степень повреждения спинного мозга;
период течения ПСМТ; характер осложнений и последствий ПСМТ.
9.1.1. Тип и характер травмы
Среди типов позвоночно-спинномозговой травмы различают изолированную, сочетанную (сопровождающуюся
повреждением органов грудной клетки, брюшной полости, переломами костей конечностей
и т.д.) и комбинированную (сочетающуюся с радиационным, термическим или химическим
поражением организма). При сочетанной и комбинированной травме в реабилитации
больных принимают участие не только неврологи и травматологи, но и хирурги,
комбустиологи и др.
По характеру повреждения позвоночно-спинномозговая травма может быть закрытой и открытой,
в зависимости от нарушения целостности кожных покровов на уровне повреждения
и, соответственно, опасности инфицирования содержимого позвоночного канала.
При закрытой ПСМТ повреждения позвоночника и повреждения спинного мозга могут
не соответствовать друг другу по степени тяжести. Так, повреждение спинного
мозга может не сопровождаться нарушением целостности костных структур позвоночника
и его связочно-суставного аппарата: например, может иметь место ушиб позвоночника
с тяжелыми неврологическими расстройствами. Травма позвоночника, в свою очередь,
может быть неосложненной (без нарушения функции спинного мозга и его корешков),
и осложненной (наряду с повреждением костных структур и связочно-суставного
аппарата имеется повреждение спинного мозга и/или его корешков). Повреждения позвоночника определяют ортопедический компонент реабилитационных мероприятий
(сохранение опорной функции позвоночника), а повреждение спинного мозга -
нейрохирургический компонент (восстановление функций спинного мозга).
Закрытые повреждения позвоночника подразделяют на следующие формы
[Бабиченко Е.И., 1994]: повреждения связочного аппарата (растяжение, разрыв),
дисков; перелом тела позвонков (линейный, компрессионный, оскольчатый, компрессионно-оскольчатый);
перелом заднего полукольца позвонков (дужек, суставных, поперечных или остистых
отростков); переломо-вывихи и вывихи позвонков, сопровождающиеся их смещением
и деформацией позвоночного канала; множественные повреждения позвоночника, сочетающиеся
друг с другом. Я.Л. Цивьян [1993] выделяет также "взрывной" перелом
тела позвонка (характеризуется интерпозицией частей поврежденного межпозвонкового
диска между фрагментами сломанного тела позвонка), проникающий перелом тела
позвонка (характеризуется повреждением замыкательной пластинки тела позвонка
и проникновением фрагментов тела позвонка в полость межпозвонкового диска).
Все закрытые повреждения позвоночника могут быть стабильными и нестабильными.
Стабильность обеспечивается целостностью дисков, костных и связочных структур
позвоночника. Повреждения на шейном уровне считаются нестабильными если
имеется смещение смежных замыкательных пластин тел больше, чем на 5 мм, или
имеется угол между нижними замыкательными пластинами двух смежных позвонков,
превышающий 11° (подобная классификация, однако, неприемлема для первых двух
шейных позвонков, на уровне которых действуют другие законы стабильности).
Для определения стабильных или нестабильных повреждений на грудном и поясничном уровнях в настоящее время пользуются теорией трехопорной структуры
позвоночника, которая предложена американским ортопедом Ф. Денисом в 1981 г.
Согласно этой теории, позвоночный столб разделен на три опорные структуры -
переднюю, среднюю и заднюю. К передней опорной структуре относятся передняя
продольная связка, передняя часть фиброзных колец дисков, передняя половина
тел позвонков вместе с диском; к средней опорной структуре - задняя продольная
связка, задняя часть фиброзных колец и задняя половина тел позвонков с диском;
к задней опорной структуре - надостистые, межостистые и желтые связки, капсулы
суставов и дуги позвонков. Нестабильными считаются такие повреждения, при которых
повреждается минимум две опорные структуры, а именно средняя и задняя. Различают
абсолютную нестабильность (возникает при переломе тел позвонков с повреждением
двух суставных отростков и при вывихах позвонков) и относительную нестабильность
(при повреждении тела и одного суставного отростка позвонка). При нестабильной
травме в результате нарушения целостности опорных комплексов может возникать
смещение позвонков по отношению друг к другу, что сопровождается угрозой сдавления
спинного мозга и его магистральных судов. Поэтому диагностика нестабильности
позвоночника чрезвычайно важна для лечебной тактики. При нестабильных повреждениях
возникает необходимость надежной внешней иммобилизации поврежденного отдела
позвоночника для предотвращения усугубления деформации позвоночного канала.
Травма шейного, верхне- и средне-грудного отделов позвоночника почти всегда
сопровождается и травмой спинного мозга; повреждения же позвонков на грудо-поясничном
и поясничном уровнях приводят к неврологической патологии лишь в 30-70% случаев
[Амелина О.А., 1998].
Закрытые травмы спинного мозга делятся на сотрясение, ушиб и сдавление
спинного мозга. Сотрясение спинного мозга характеризуется обратимыми
сегментарными и легкими проводниковыми нарушениями, которые самостоятельно или
после лечения полностью или почти полностью исчезают в течение первых 5-7 суток. Ушиб спинного мозга характеризуется возникновением как обратимых, так
и необратимых изменений. Может наблюдаться морфологический перерыв спинного
мозга - анатомический, с расхождением концов и наличием между ними диастаза,
и аксональный, когда при внешней сохранности спинного мозга разрушены его проводниковые
системы. Клинически ушиб проявляется синдромами частичного или полного нарушения
проводимости спинного мозга. Степень необратимости изменений определяется по
мере ликвидации явлений спинального шока. Некоторые авторы выделяют различные
степени ушиба спинного мозга. Ушиб спинного мозга легкой степени характеризуется
синдромом частичного нарушения проводимости, при этом восстановление функций
почти полное и происходит в течение месяца; ушиб средней степени проявляется
синдромом частичного или полного нарушения проводимости с неполным восстановлением
функций в течение 2-3 месяцев; ушиб тяжелой степени характеризуется незначительным
улучшением функций либо сохранением синдрома полного нарушения проводимости
[Амелина О.А., 1998]. Сдавление спинного мозга, вызываемое обычно костными
отломками позвонков, фрагментами связок и дисков, оболочечной или внутримозговой
гематомой, отеком, приводит к возникновению в спинном мозге очагов некроза и
клинически проявляется синдромами частичного либо полного нарушения проводимости.
Если при сотрясении и ушибе спинного мозга проводится консервативное лечение,
то при сдавлении спинного мозга возникают экстренные показания к устранению
компрессии хирургическими или консервативными методами.
Открытые повреждения (неогнестрельные и огнестрельные) по признаку целостности
твердой мозговой оболочки делят на непроникающие (твердая мозговая оболочка
сохранна) и проникающие (повреждение твердой мозговой оболочки). Поскольку твердая
мозговая оболочка служит барьером, препятствующим проникновению инфекции в подоболочечное
пространство, проникающие повреждения сопровождаются высоким риском развития
инфекционных осложнений со стороны центральной нервной системы. Проникающие
повреждения устанавливают либо по наличию ликвореи, либо при выполнении оперативного
вмешательства, когда налицо повреждение твердой мозговой оболочки. Клинически
открытые повреждения могут сопровождаться синдромом частичного или полного нарушения
проводимости спинного мозга.
9.1.2. Степень и уровень повреждения спинного мозга
Степень повреждения спинного мозга относится к одним из решающих прогностических
факторов. Различают частичное повреждение спинного мозга и полное его повреждение,
или морфологический перерыв (анатомический либо аксональный). Дифференциальная
диагностика частичного и полного повреждения спинного мозга в остром периоде
травмы нередко затруднительна. Частичное нарушение функций всегда свидетельствует
о частичном повреждении спинного мозга. В то же время полное нарушение проводимости
в остром периоде может сопровождать как частичное повреждение, так и полный
перерыв спинного мозга; при этом окончательное заключение о степени повреждения
можно сделать лишь в более поздние сроки, по мере ликвидации явлений спинального
шока. Поэтому в остром периоде позвоночно-спинномозговой травмы целесообразнее говорить о синдроме полного
либо неполного (частичного) нарушения проводимости спинного мозга. Синдром
частичного нарушения проводимости характеризуется нарушениями проводниковых
функций в виде пареза или паралича мышц, тазовыми и чувствительными расстройствами,
на фоне которых имеются признаки, свидетельствующие о частичной сохранности
проводимости спинного мозга (наличие каких-либо движений и/или чувствительности
ниже уровня поражения). При синдроме полного нарушения проводимости таких
признаков не имеется. Наиболее точным признаком полного поражения спинного мозга
считают отсутствие чувствительных и двигательных функций в сакральных сегментах,
в иных случаях нарушение проводимости является неполным [Waters R. и соавт.,
1993]. Американская Ассоциация Спинальной Травмы (American Spinal Injury Association)
разработала 5-ранговую шкалу степени нарушения проводимости спинного мозга [1992]:
рангу "А" (полное нарушение проводимости) соответствует отсутствие
сенсорных и моторных функций в сегментах S4-S5;
рангу "В" (неполное нарушение) - наличие ниже уровня поражения (в
том числе в сегментах S4-S5) чувствительности при отсутствии движений;
рангу "С" (неполное нарушение) - наличие ниже уровня поражения движений
при силе большинства ключевых мышц менее 3-х баллов;
рангу "Д" (неполное нарушение) - наличие ниже уровня поражения движений
при силе большинства ключевых мышц 3 балла и более;
рангу "Е" (норма) - полная сохранность чувствительных и двигательных
функций.
Определение степени нарушения проводимости имеет важное прогностическое значение.
Чем больше изначальная сохранность двигательных функций, тем обычно быстрее
и полнее идет восстановление [Maynard F. и соавт., 1979]. Так, если через месяц
после травмы сила мышц составляет 0 баллов, то через год достижения силы в 3
балла можно ожидать лишь в 25% случаев; если через месяц сила мышц составила
1-2 балла, то через год она обычно возрастает до 3-х баллов; у больных с полной
тетраплегией, сохраняющейся к концу 1-го месяца после травмы, редко можно ожидать
существенного улучшения функций нижних конечностей [Waters R. и соавт., 1989;
1993].
Отдельно необходимо остановиться на понятии спинального шока. Патогенетические
и патофизиологические механизмы спинномозгового (спинального) шока до конца
не выяснены. Клинически он выражается в атоническом параличе, арефлексии, анестезии
всех видов чувствительности ниже уровня травмы, а в некоторых случаях и на 2-3
сегмента выше этого уровня, отсутствии функций тазовых органов, быстром присоединении
трофических расстройств. Это происходит в результате травматического перераздражения
спинного мозга или лишения супраспинального влияния на него со стороны среднего
и продолговатого мозга с нарушением межнейрональных связей. Для спинального
шока характерна обратимость неврологических нарушений в остром и раннем периодах
позвоночно-спинномозговой травмы. Глубина и продолжительность шока зависят от
тяжести травмы. Первыми признаком окончания спинномозгового шока являются восстановление
бульбокавернозного рефлекса и смыкания ануса.
Спинальный шок поддерживается или даже углубляется, если не ликвидированы сдавление
спинного мозга и нестабильность позвоночника. Поддерживают спинальный шок и
воспалительные осложнения со стороны мочевыводящих путей, легких, а также гемодинамические
расстройства. В этих случаях шок может длиться месяцами и даже годами, поддерживая
и углубляя образовавшиеся пролежни, препятствуя выработке спинального автоматизма
функции тазовых органов. Наличие или отсутствие спинального шока никоим образом
не влияет на вопросы показаний или противопоказаний к оперативному лечению позвоночно-спинномозговой
травмы.
Уровень травмы спинного мозга (кранио-спинальный, шейное утолщение,
грудной отдел, поясничное утолщение, конус и корешки конского хвоста) определяет
распространенность клинических проявлений и, соответственно, способность больного
к самообслуживанию и передвижению, прогноз восстановления его нормальной жизнедеятельности
(таблица 9.1). Необходимо учитывать, что травма может сопровождаться
повреждением спинного мозга не только в месте приложения травмирующей силы,
но и на отдалении вследствие расстройств крово- и лимфообращения, развития травматического
миелита. Поэтому важно определить неврологический уровень поражения, под которым
понимают наиболее каудальный сегмент спинного мозга, который еще обеспечивает
нормальную двигательную и чувствительную иннервацию обеих сторон тела [Yarkony
G., Chen D., 1996].
Таблица 9.1. ФУНКЦИОНАЛЬНОЕ ЗНАЧЕНИЕ УРОВНЯ ПОВРЕЖДЕНИЯ
СПИННОГО МОЗГА
(по J. Ditunno)
Активность
|
Уровень повреждения (сегменты спинного мозга) |
С5 |
С6 |
С7 |
Т1 |
Т6 |
Т12 |
L4 |
Самообслуживание |
| прием пищи |
- |
± |
+ |
+ |
+ |
+ |
+ |
| одевание |
- |
- |
± |
+ |
+ |
+ |
+ |
туалет
|
- |
- |
± |
+ |
+ |
+ |
+ |
Перемещение в постели |
повороты в постели
|
- |
± |
+ |
+ |
+ |
+ |
+ |
сидение в постели
|
- |
- |
± |
+ |
+ |
+ |
+ |
| Пользование креслом-каталкой: перемещение в
кресло и из кресла |
- |
± |
± |
+ |
+ |
+ |
+ |
| Ходьба |
- |
- |
- |
- |
± |
+ |
+ |
| Работа по дому (ручная) |
- |
- |
+ |
+ |
+ |
+ |
+ |
| Работа вне дома |
- |
- |
- |
± |
± |
+ |
+ |
| Вождение автомобиля |
- |
- |
- |
± |
+ |
+ |
+ |
| Пользование общественным транспортом |
- |
- |
- |
- |
- |
± |
+ |
Аббревиатуры: "+" - возможно, "-" - невозможно, "±"
- невозможно
Травма спинного мозга на уровне шейных позвонков характеризуется преобладанием
тяжелых видов повреждения (ушиб, сдавление, гематомиелия) и высокой летальностью
(от 35 до 70%) [Луцик А.А, 1994]. Повреждение на уровне С1-С4 сегментов спинного
мозга (кранио-спинальный переход) вызывает так называемую "высокую"
тетраплегию, сопровождающуюся не только двигательными нарушениями в верхних
и нижних конечностях, чувствительными и тазовыми расстройствами, но и нарушением
дыхания вследствие денервации диафрагмы, межреберных и абдоминальных мышц. Выжившие
больные с тяжелой травмой выше уровня С4 нуждаются в искусственной вентиляциии
и лишены малейшей возможности самообслуживания. Неврологический уровень повреждения
шейного утолщения спинного мозга, соответствующий сегменту С5, характеризуется
возможностью сгибания руки в локтевом суставе; уровень С6 - возможностью сгибания
в локтевом суставе и радиального разгибания кисти в кистевом суставе; уровень
С7 - возможностью сгибания и разгибания руки в локтевом суставе, разгибания
и сгибания кисти в кистевом суставе, разгибания пальцев; уровень С8 - дополнительно
к вышеуказанному, сохранностью сгибания пальцев.
Повреждения грудного отдела спинного мозга характеризуются параличом
или парезом ног (в период спинального шока - вялым, затем - спастическим), нарушением
чувствительности ниже уровня поражения по проводниковому типу, тазовыми проводниковыми
расстройствами. Повреждение верхнегрудного отдела спинного мозга приводит к
нарушению функции дыхательных мышц грудной клетки, что сопровождается резким
ослаблением дыхания. Повреждение на уровне Th3-Th5 сегментов может сопровождаться
нарушением сердечной деятельности, поскольку эти сегменты осуществляют иннервацию
сердца. Повреждения на верхне- и среднегрудном уровнях сопровождаются параличом
мышц спины, на уровне Тh10-12 сегментов - параличом мышц брюшного пресса. При
уровне повреждения ниже Тh12 дыхательная функция обычно не страдает. Восстановление
двигательных функций нижних конечностей при клинике полного поражения спинного
мозга выше уровня Тh9 маловероятно. Чем каудальнее уровень поражения, тем более
вероятно восстановление функции мышц ног, в особенности в сгибателях бедра и
разгибателях голени. При неврологическом уровне поражения, соответствующем Тh1
сегменту и ниже, сохраняется функция рук, что обеспечивает больному возможность
самообслуживания и передвижения в велоколяске. При уровне поражения Тh12 и ниже
велика вероятность того, что больной научиться вставать на ноги и передвигаться
без помощи велоколяски [Waters R.. и соавт., 1992].
Повреждения поясничного утолщения вызывают вялый паралич всех или только
дистальных отделов ног, выпадение чувствительности ниже уровня повреждения,
нарушения функций тазовых органов. Изолированное повреждение конуса спинного
мозга (сегменты S2-5) характеризуется нарушением функции тазовых органов по
периферическому типу и нарушением чувствительности в аногенитальной области.
У этих больных потенциал к восстановлению ходьбы наибольший. К признакам, указывающим
на благоприятный в отношении восстановления ходьбы прогноз, относят сохранность
функции мышц таза, возможность сгибания ног в тазобедренных суставах, сохранность
функции четырехглавой мышцы бедра, хотя бы на одной стороне, а также наличие
проприоцептивной чувствительности в тазобедренных и голеностопных суставах;
при этом слабость разгибателей и абдукторов бедер может быть скомпенсирована
с помощью костылей, а слабость мышц, осуществляющих движения в голеностопном
суставе - с помощью фиксирующих аппаратов для этого сустава [Hussey R., Stauffer
Е., 1973]. С целью прогнозирования восстановления ходьбы Waters R. и соавторы
[1989] предложили использовать "амбулаторный индекс двигательной функции"
(Ambulatory Motor Index), согласно которому по 4-х балльной шкале (0-паралич,
1 - выраженный парез, 2 - умеренный парез, 3 - легкий парез или норма) с обеих
сторон оценивается функция сгибателей, абдукторов и разгибателей бедра, сгибателей
и разгибателей голени. Максимальная сумма баллов при тестировании указанных
5 групп мышц с обеих сторон составляет 30 баллов. При суммарной оценке, равной
79% и более этой максимальной суммы, прогнозируется восстановление ходьбы без
помощи вспомогательных средств; при оценке 60-78% - восстановление ходьбы с
помощью одного аппарата, фиксирующего ногу в коленном и голеностопном суставах;
при оценке менее 40% прогнозируется потребность в двух фиксирующих аппаратах.
Таким образом, правильное определение уровня и степени повреждения спинного
мозга представляется чрезвычайно важным. Для этого необходимо очень детальное
исследование чувствительности и двигательных функций больного. Американской
Ассоциацией спинальной травмы разработан специальный стандарт обследования больно
го с ПСМТ и оценки степени повреждения спинного мозга (рис.9.1).
Обследование имеет целью выявить наиболее каудальный уровень, на котором чувствительные
и двигательные функции еще сохранены с обеих сторон. Для этого с каждой стороны
(справа и слева) исследуются 10 миотомов и 28 дерматомов. На рис. 9.1 указаны
ключевые мышечные группы для каждого миотома. Сила мышц оценивается по 5-балльной
системе: от 0 баллов, соответствующих параличу, до 5 баллов, соответствующих
норме. Мышцы исследуются в направлении от ростральных к каудальным сегментам.
Иннервация мышц, сила которых оценивается в 3 балла, может считаться сохранной
в тех случаях, когда сила непосредственно предшествующих им (более ростральных)
ключевых) мышц оценивается в 4-5 баллов [Yarkony G., Chen D., 1996]. Для каждого
дерматома на рисунке указаны ключевые точки чувствительности. Общая оценка двигательной
функции производится путем суммирования результатов тестирования 10 ключевых
мышечных групп с обеих сторон, общая оценка чувствительности - путем суммирования
результатов болевой и тактильной чувствительности с обеих сторон. Стандартное
тестирование, проводимое в динамике, помогает осуществлять контроль за восстановлением
нарушенных функций а также имеет прогностическое значение. Так, если оценка
двигательной функции нижних конечностей (по пять ключевые мышечных групп справа
и слева) к концу 1-го месяца после травмы превышает 15 баллов, то к концу 1-го
года можно ожидать восстановление ходьбы, хотя бы с помощью вспомогательных
приспособлений. Восстановление двигательных функций у больных с тетраплегией
более вероятна при сохранности в сакральных сегментах болевой чувствительности
[Crozier К. и соавт., 1992]. Если к концу 1-го месяца у больного с тетраплегией
сила сгибателей предплечья была равна 0, то ожидать восстановления мышечной
силы разгибателей кисти не приходится; если же к этому времени сила сгибателей
предплечья достигает 1-2-х баллов, то можно предположить восстановление силы
мышц, осуществляющих разгибание в кистевом суставе, до 3-х баллов. Если сила
мышц, разгибающих руку в локтевом суставе, к концу 1-го месяца достигла 1-2-х
баллов, то через год она обычно превышает 3 балла [Waters R. и соавт., 1993].
9.1.3. Периоды позвоночно-спинномозговой травмы
В течении ПСМТ выделяют следующие периоды, которые отражают динамику
деструктивных и восстановительных процессов [Раздольский И.Я., 1963].
Острый период - первые 2-3 суток; характеризуется некротическими и некробиотическими
изменениями в спинном мозге, как за счет непосредственного повреждения и отека
спинного мозга, так и в результате расстройства крово- и лимфообращения. Клинически
может проявляться картиной спинального шока; синдром полного нарушения проводимости
в этот период наблюдается как при полном, так и при частичном повреждении спинного
мозга. В тех случаях, когда возникший тотчас после травмы синдром полного нарушения
проводимости спинного мозга стойко сохраняется, и в течение первых 24-48 часов
не наступает хотя бы минимальный регресс двигательных и чувствительных расстройств,
рассчитывать на восстановление утраченных функций практически не приходится
[Меламуд Э.Е., 1994].
Ранний период продолжается последующие 2-3 недели. Морфологически характеризуется
очищением очагов первичного травматического некроза признаками деструктивных
изменений в нервных волокнах и нервных пучках, первыми признаками репаративных
процессов. Клинически проявляется синдромом полного или частичного нарушения
проводимости спинного мозга. К концу этого периода обратимые изменения в спинном
мозге обычно исчезают.
Промежуточный период - длится до 3-4 месяцев. Морфологически наблюдаются
организация дефекта, начальное формирование соединительнотканного рубца и кист,
признаки регенерации нервных волокон. Клинически в начале этого периода полностью
исчезают явления спинального шока и обратимые изменения, выявляется истинный
характер повреждения спинного мозга.
Поздний период - начинается с 3-4-х месяцев и продолжается неопределенно
долгое время. Морфологически характеризуется заключительной фазой рубцевания
и формирования кист, продолжающимися деструктивными и репаративными процессами
в нервной ткани.
В случаях морфологического перерыва спинного мозга развивается автоматизация
его отделов, расположенных книзу от уровня перерыва. В случаях частичного повреждения
спинного мозга наблюдается медленное восстановление функций. Необходимо отметить,
что регенерация клеточных и проводниковых систем спинного мозга невозможна;
лишь корешки конского хвоста в ряде случаев способны к регенерации [Савченко
А.Ю., 1994]. Восстановление функций происходит за счет сохранившихся клеток
и волокон после устранения парабиотического состояния нервных клеток, ликвидации
отека и циркуляторных расстройств. Восстановление функции тазовых органов возможно
благодаря выработке автоматизма их деятельности за счет растормаживания сегментов
спинного мозга, расположенных дистальнее уровня поражения, а также за счет механизмов
компенсации (проведение импульсов от вышележащих отделов через пограничный симпатический
ствол). Что касается двигательных функций, то к концу первых 6 месяцев темп
их восстановления значительно замедляется и выходит на "плато" [Welsh
R. и соавт., 1986]. В некоторых случаях (развитие соединительнотканного рубца
в очаге поражения, приводящее к сдавлению спинного мозга, либо прогрессирующая
деформация позвоночника) может наступить ухудшение функций. Помимо сохраняющейся
компрессии спинного мозга или прогрессирующего спаечного оболочечного процесса,
к усугублению имевшегося неврологического дефицита либо к появлению новых симптомов
может приводить и прогрессирующая миелопатия [Макаров А.Ю., Амелина О.А., 1998].
Морфологически в основе прогрессирующей миелопатии могут лежать атрофия спинного
мозга (локальная или диффузная), миеломаляция (очаги некроза, глиоза), кистозная
дегенерация (микро- и макрокисты). Клинически прогрессирующая травматическая
болезнь может проявляться:
а) синдромами миелопатии (сиринго-миелитический синдром, синдром бокового амиотрофического
склероза, спастическая параплегия, нарушения спинального кровообращения);
б) спинальным арахноидитом, характеризующимся полирадикулярным болевым синдромом,
усугублением имевшихся проводниковых расстройств;
в) дистрофическим процессом в виде остеохондроза, деформирующего спондилеза
со стойким болевым синдромом.
Существуют и иные классификации периодов течения ПСМТ. Так, А.Ю. Макаров и
О. А. Амелина [1998] выделяют острый период (от нескольких дней до 3-4 месяцев),
промежуточный, или восстановительный (продолжительностью 1-2 года) и поздний
(может продолжаться неопределенно долго).
9.1.4. Осложнения и последствия повреждений позвоночника и спинного мозга
Осложнения и последствия повреждений позвоночника и спинного мозга делят следующим
образом [Бабиченко Е.И., 1994; Yarkony G., Chen D., 1996]:
1) инфекционно-воспалительные осложнения;
2) нейротрофические и сосудистые нарушения;
3) нарушения функции тазовых органов;
4) ортопедические последствия.
Инфекционно-воспалительные осложнения могут быть ранними (развиваются
в острый и ранний периоды ПСМТ) и поздними. В остром и раннем периоде гнойно-воспалительные
осложнения в первую очередь связаны с инфицированием дыхательной и мочевыводящей
систем, а также с пролежневым процессом, который протекает по типу гнойной раны.
При открытой ПСМТ возможно также развитие таких грозных осложнений, как гнойный
эпидурит, гнойный менингомиелит, абсцесс спинного мозга, остеомиелит костей
позвоночника. К поздним инфекционно-воспалительным осложнениям относят хронический
эпидурит и арахноидит.
Нейротрофические и сосудистые нарушения возникают в связи с денервацией
тканей и органов. В мягких тканях у больных ПСМТ очень быстро развиваются пролежни
и плохо заживающие трофические язвы. Пролежни и язвы становятся входными воротами
инфекции и источниками септических осложнений, приводя в 20-25% случаев к смерти
[Гайдар Б.В. и соавт., 1997].
Для анатомического перерыва спинного мозга характерно возникновение так называемых
твердых отеков нижних конечностей. Характерны нарушения метаболизма (гипопротеинемия,
гиперкальциемия, гипергликемия), остеопороз, анемия. Нарушение вегетативной
иннервации внутренних органов приводит к развитию гнойно-некротических язвенных
колитов, энтероколитов, гастритов, к острым желудочно-кишечным кровотечениям,
к дисфункции печени, почек, поджелудочной железы. Наблюдается тенденция к камнеобразованию
в желчных и в мочевыводящих путях. Нарушение симпатической иннервации миокарда
(при травмах шейного и грудного отделов спинного мозга) проявляется брадикардией,
аритмией, ортостатической гипотензией. Может развиться либо усугубиться ишемическая
болезнь сердца, при этом больные могут не чувствовать боли в результате нарушения
ноцептивной афферентной импульсации от сердца [Arrowood J. и соавт., 1987].
Со стороны легочной системы более чем у 60% больных в раннем периоде развивается
пневмония, которая служит одной из наиболее частых причин гибели пострадавших
[De Vivo М. и соавт., 1993].
Другим грозным осложнением, приводящим нередко к летальному исходу, является тромбоз глубоких вен, возникающий по различным данным у 47-100% больных
ПСМТ [Merli G. и соавт., 1988]. Наиболее высок риск тромбоза глубоких вен в
первые 2 недели после травмы. Следствием тромбоза глубоких вен может стать эмболия
легочной артерии, которая возникает в среднем у 5 % больных и является ведущей
причиной смерти при ПСМТ [Waring W., Karunas R., 1991]. При этом по причине
повреждения спинного мозга могут отсутствовать типичные клинические симптомы
эмболии (боль в груди, диспноэ, кровохарканье); первыми признаками могут быть
нарушения сердечного ритма [Fluter G., 1993]. Диагностические мероприятия при
подозрении на тромбоз глубоких вен или эмболию ветвей легочной артерии описаны
в главе 5.
Реабилитологу необходимо знать и еще об одном осложнении - вегетативной
дизрефлексии. Вегетативная дизрефлексия представляет собой мошную симпатическую
реакцию, возникающую в ответ на болевые или иные стимулы у больных с уровнем
поражения спинного мозга выше Тh6 (т.е. выше отхождения ветвей поясничной части
симпатического ствола). У больных с тетраплегией этот синдром наблюдается, по
данным разных авторов, в 48- 83% случаев, обычно спустя 2 и более месяцев после
травмы [Lindan R. и соавт., 1980]. Причиной служит болевая либо проприоцептивная
импульсация, обусловленная растяжением мочевого пузыря, катетеризацией, гинекологическим
или ректальным обследованием, а также другими интенсивными воздействиями. В
норме проприоцептивные и болевые импульсы следуют к коре головного мозга по
задним столбам спинного мозга и спиноталамическому пути. Полагают, что при перерыве
этих путей импульсация циркулирует на спинальном уровне, вызывая возбуждение
симпатических нейронов и мощный "взрыв" симпатической активности;
при этом нисходящие супраспинальные ингибирующие сигналы, в норме модулирующие
вегетативную реакцию, в силу повреждения спинного мозга не оказывают должного
тормозного воздействия [Erickson R., 1980]. В результате развивается спазм периферических
сосудов и сосудов внутренних органов, что приводит к резкому подъему артериального
давления. Нескорригированная гипертензия может привести к потере сознания, к
развитию внутримозгового кровоизлияния, острой сердечной недостаточности.
К достаточно частому осложнению ПСМТ относится гетеротопическая оссификация,
развивающаяся обычно в первые 6 месяцев после травмы, по различным данным, у
16-53% больных [Venier L., Ditunno J., 1971]. Эктопические оссификаты появляются
лишь в областях, расположенных ниже неврологического уровня поражения. Обычно
поражаются области крупных суставов конечностей (тазобедренные, коленные, локтевые,
плечевые).
Нарушения функции тазовых органов проявляются расстройствами мочеиспускания
и дефекации. В стадию спинального шока наблюдается острая задержка мочи, связанная
с глубокой депрессией рефлекторной активности спинного мозга. По мере выхода
из шока форма нейрогенной дисфункции мочевого пузыря зависит от уровня поражения
спинного мозга. При поражении надсегментарных отделов (мочевой пузырь
получает парасимпатическую и соматическую иннервацию из сегментов S2-S4) развивается
нарушение мочеиспускания по проводниковому типу. Вначале наблюдается задержка
мочеиспускания, связанная Т повышением тонуса наружного сфинктера мочевого пузыря.
Может наблюдаться парадоксальная ишурия - при переполненном мочевом пузыре моча
выделяется по каплям в результате пассивного растяжения шейки мочевого пузыря
и пузырных сфинктеров. По мере развития автоматизма отделов спинною мозга, находящихся
дистальнее уровня поражения (спустя 2-3 недели после травмы, а иногда и в более
отдаленные сроки), формируется "рефлекторный" (иногда его называют
"гиперрефлекторный") мочевой пузырь: начинает работать спинальный
центр мочеиспускания, локализующийся в конусе спинного мозга, и мочеиспускание
происходит рефлекторно, по типу автоматизма, в ответ на наполнение мочевого
пузыря и раздражение рецепторов его стенок, при этом нет произвольной (корковой)
регуляции мочеиспускания. Наблюдается недержание мочи. Моча выделяется внезапно,
небольшими порциями. Может наблюдаться парадоксальное прерывание мочеиспускания
в связи с непроизвольным преходящим торможением мочевого потока в течение рефлекторного
опорожнения. При этом императивный позыв на опорожнение мочевого пузыря указывает
на неполное нарушение проводимости спинного мозга (сохранность афферентных проводящих
путей от пузыря к коре больших полушарий), тогда как спонтанное внезапное опорожнение
мочевого пузыря без позыва - на полное нарушение проводимости спинного мозга.
На неполное поражение проводящих путей указывает также ощущение самого процесса
мочеиспускания и ощущение облегчения после мочеиспускания (сохранность путей
температурной, болевой и проприоцептивной чувствительности от уретры к коре
головного мозга). При надсегментарном поражении положителен тест "холодной
воды": через несколько секунд после введения через уретру в мочевой пузырь
60 мл холодной воды вода, а иногда и катетер, с силой выталкиваются наружу.
Повышен также тонус наружного ректального сфинктера. С течением времени в стенках
мочевого пузыря могут наступить дистрофические и рубцовые изменения, приводящие
к гибели детрузора и формированию вторично-сморщенного мочевого пузыря ("органический
арефлекторный мочевой пузырь"). При этом наблюдается отсутствие пузырного
рефлекса, развивается истинное недержание мочи.
При травме спинного мозга с непосредственным поражением спинальных центров мочеиспускания (крестцовых сегментов S2-S4) происходит угасание рефлекса опорожнения
мочевого пузыря в ответ на его наполнение. Развивается гипорефлекторная форма
мочевого пузыря ("функциональный арефлекторный мочевой пузырь"), характеризующаяся
низким внутрипузырным давлением, снижением силы детрузора и резко заторможенным
рефлексом мочеиспускания. Сохранность эластичности шейки мочевого пузыря приводит
к перерастяжению мочевого пузыря и большому количеству остаточной мочи. Характерно
напряженное мочеиспускание (для опорожнения мочевого пузыря больной натуживается
или производит ручное выдавливание). Если больной перестает напрягаться, опорожнение
прекращается (пассивное прерывистое мочеиспускание). Тест "холодной воды"
отрицателен (рефлекторный ответ в виде выталкивания введенной в мочевой пузырь
воды не наблюдается в течение 60 секунд). Анальный сфинктер расслаблен. Иногда
пузырь опорожняется автоматически, но не за счет спинальной рефлекторной дуги,
а в связи с сохранением функции интрамуральных ганглиев. Необходимо отметить,
что чувство растяжения мочевого пузыря сохраняется даже при полном повреждении
спинного мозга в пояснично-крестцовом отделе благодаря симпатической иннервации,
которая распространяется до верхних грудных сегментов (симпатическая иннервация
мочевого пузыря связана с сегментами Тh11, Тh12, L1, L2). По мере развития в
мочевом пузыре дистрофических процессов и потери шейкой пузыря эластичности
формируются органический арефлекторный мочевой пузырь и истинное недержание
с постоянным выделением мочи по мере ее поступления в пузырь.
Для определения формы и степени нарушения функции мочевого пузыря по прошествии
спинального шока с целью выбора методов лечения необходимо использование целого
комплекса урологических исследований.
Нейроурологическая характеристика функционального состояния мочевого пузыря
и почек должна включать детальные сведения об акте мочеиспускания, о взаимоотношении
тонуса детрузора и сфинктера, морфологических изменениях в стенке мочевого пузыря,
а также данные о мочеобразовательной и мочевыделительной функциях почек. С этой
целью прежде всего определяют количество мочи, выделяемой однократно при сохранившемся
мочеиспускании, а также количество остаточной мочи и емкость мочевого пузыря.
Затем проводят урологическое обследование - сфинктерометрию, цистометрию, цистоуретрографию,
цистоскопию, измерение скорости потока мочи. Эти методы позволяют оценить высоту
пузырного рефлекса, объем мочевого пузыря и количество остаточной мочи, тонус
мочевого пузыря, собственную силу детрузора. Необходим также лабораторный и
бактериологический анализ мочи и соответствующие биохимические анализы крови
(остаточный азот, мочевина). При необходимости проводят изотопную ренографию,
ультразвуковое исследование почек.
Для выполнения сфинктеро- и цистометрии существуют специальные приборы, выпускаемые
в основном зарубежными фирмами. Можно пользоваться и более простыми приспособлениями,
с помощью которых возможно определение рефлекторной сократительной функции и
тонической активности мочевого пузыря и его замыкательного аппарата.
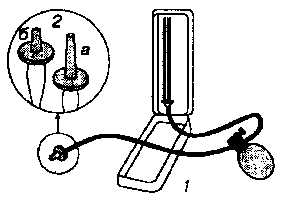
Сфинктерометрия основана на измерении давления, необходимого для преодоления
запирательных механизмов ретроградно вводимым в уретру воздухом или жидкостью.
Для исследования суммарного сопротивления замыкательного аппарата мочевого пузыря
в уретру нагнетается воздух аппаратом для измерения артериального давления,
соединенным с уретрой специальным наконечником и переходной резиновой трубкой
(рис.9.2). Тонус сфинктера фиксируется в момент прорыва воздуха через
сфинктер в мочевой пузырь по характерному хлопающему звуку.
Цистометрия или цистоманометрия может быть определена путем измерения высоты
пузырного давления водным манометром при различных степенях фракционного наполнения
мочевого пузыря теплым (37°) раствором фурацилина в концентрации 1:5000 (рис.9.3).
 |
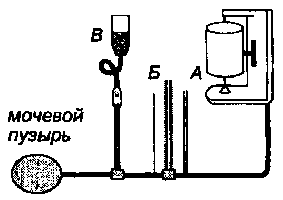 |
Рис. 9.2. Схема аппарата
для сфинктерометрии:
1 - аппарат Рива-Рочи, 2 - наконечники, вставляющиеся в уретру (2а - для
мужчин, 2б -для женщин) (О.А.Перльмуттер, 2000) |
Рис. 9.3. Схема аппарата
для цистоманометрии: А - кимограф, Б - водяной манометр, В - капельница
с фурацилином (О.А.Перльмуттер, 2000) |
Нулевой пункт манометра устанавливается на уровне мочевого пузыря. Регистрация
внутрипузырного давления производится при наполнении мочевого пузыря порциями
по 50 мл фурацилина. Наполнение производят до появления сильного позыва на мочеиспускание.
Если такой позыв отсутствует, то вводят не более 600-700 мл раствора. На кимографе
регистрируются волнообразные линии, которые вдруг внезапно увеличиваются по
амплитуде, это признак того, что детрузор начал сокращаться в ответ на раздражение
его стенки вводимой жидкостью. Одновременно с появлением этих высокоамплитудных
колебательных движений на водяном манометре образуется короткий пиковый подъем,
амплитуда которого характеризует тонус детрузора. Введенное количество раствора
обозначает эффективную мощность мочевого пузыря. Данные внутрипузырного давления,
определяемые по манометру, сопоставляют с данными эффективной мощности пузыря,
при этом получают графическое изображение (рис.9.4).
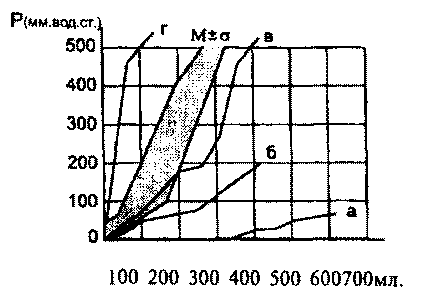 |
| Рис. 9.4. Различные типы цистометрических кривых
у больных с травмами позвоночника и спинного мозга: а - атонический, б -
гипотонический, в - нормотонический, г - гипертонический (О.А.Перльмуттер,
2000) |
При выделении клинических синдромов основное значение придается тонусу детрузора
и сфинктера и их взаимоотношению. Тонус детрузора или силу его сокращения измеряют
по приросту внутрипузырного давления в ответ на введение всегда постоянного
количества жидкости - 50 мл, если этот прирост составляет 103±13 мм водн. ст.,
тонус детрузора мочевого пузыря считается нормальным, при меньшем приросте -
сниженным, при большем - повышенным. Нормальными показателями сфинктерометрии
считаются 70-110 мм рт.ст.
В зависимости от соотношения состояния детрузора и сфинктера выделяют несколько
синдромов.
Атонический синдром отмечается чаще при поражении конуса спинного мозга,
т.е. спинальных центров регуляции мочеиспускания. При цистометрическом исследовании
введение в мочевой пузырь 100-450 мл жидкости не изменяет нулевого пузырного
давления. Введение больших объемов (до 750 мл) сопровождается медленным повышением
внутрипузырного давления, но оно не превышает 80-90 мм водн. ст. Сфинктерометрия
при атоническом синдроме выявляет низкие показатели тонуса сфинктера - 25-30
мм рт.ст. Клинически это сочетается с атонией и арефлексией скелетной мускулатуры.
Синдром гипотонии детрузора - также результат сегментарных дисфункций
мочевого пузыря, при этом вследствие снижения тонуса детрузора емкость пузыря
увеличивается до 500-700 мл. Тонус сфинктера может быть пониженным, нормальным
и даже повышенным.
Синдром преобладающей гипотонии сфинктера наблюдается при травмах на
уровне S2-S4 сегментов; для него характерно частое непроизвольное отделение
мочи без позыва. При сфинктерометрии выявляется отчетливое снижение тонуса сфинктера
и на цистограмме - незначительно сниженный или нормальный тонус детрузора. При
пальпаторном исследовании сфинктера прямой кишки и мышц промежности определяется
низкий тонус.
Синдром гипертонии детрузора и сфинктера отмечается у больных с проводниковым
типом дисфункции мочевого пузыря. Цистометрически при введении в мочевой пузырь
50-80 мл жидкости наблюдается резкий скачок внутрипузырного давления до 500
мм водн. ст. При сфинктерометрии тонус его высокий - от 100 до 150 мм рт. ст.
Наблюдаются резкие сокращения мышц промежности в ответ на их пальпацию.
Синдром преобладающей гипертонии детрузора при цистометрии характеризуется
повышением тонуса детрузора при маленькой емкости пузыря (50- 150 мл), отмечается
высокий скачок внутрипузырного давления в ответ на введение 50 мл жидкости,
а тонус сфинктера может быть нормальным, повышенным или пониженным.
Для выяснения электровозбудимости мочевого пузыря применяют также трансректальную
электростимуляцию. При грубых дистрофических процессах в мочевом пузыре детрузор
теряет свою возбудимость, что проявляется отсутствием подъема внутрипузырного
давления в ответ на электрическую стимуляцию. Степень дистрофических процессов
определяют по количеству коллагеновых волокон методом пузырной биопсии (при
инфицировании мочевых путей либо значительных трофических нарушениях в стенке
пузыря биопсия не показана).
Нарушение акта дефекации при ПСМТ также зависит от уровня поражения спинного
мозга. При надсегментарном поражении больной перестает ощущать позывы
на дефекацию и наполнение прямой кишки, наружный и внутренний сфинктеры прямой
кишки находятся в состоянии спазма, возникает стойкая задержка стула. При поражении спинальных центров развивается вялый паралич сфинктеров и нарушение рефлекторной
перистальтики кишечника, что проявляется истинным недержанием кала с его отхождением
небольшими порциями при поступлении в прямую кишку. В более отдаленный период
может наступать автоматическое опорожнение прямой кишки за счет функционирования
интрамурального сплетения.
При ПСМТ возможно также возникновение гипотонического запора, связанного с
гипомобильностью больного, слабостью мышц брюшного пресса, парезом кишечника.
Нередко наблюдаются геморроидальные кровотечения [Cosman В. и соавт., 1993].
Ортопедические последствия ПСМТ могут быть следующими [Соленый В.И.,
1994]: нестабильность травмированного отдела позвоночника; сколиозы и кифозы
позвоночника (особенно склонны к прогрессированию кифотические деформации с
углом кифоза, превышающим 18-20°); вторичные вывихи, подвывихи и патологические
переломы; дегенеративные изменения в межпозвонковых дисках, суставах и связках
позвоночника; деформация и сужение позвоночного канала с компрессией спинного
мозга. Данные последствия сопровождаются обычно стойким болевым синдромом, ограничением
подвижности травмированного отдела позвоночника и его функциональной несостоятельностью,
а в случаях сдавления спинного мозга - прогрессирующим нарушением функций спинного
мозга. Возникшие ортопедические нарушения при отсутствии своевременного лечения
часто прогрессируют и приводят больного к инвалидности.
9.2. РЕАБИЛИТАЦИЯ В ОСТРОМ И РАННЕМ ПЕРИОДАХ ПОЗВОНОЧНО-СПИННОМОЗГОВОЙ
ТРАВМЫ
9.2.1. Острый период
В остром периоде ПСМТ все мероприятия направлены на спасение жизни больного
и на предупреждение усугубления повреждения содержимого позвоночного канала.
С этой целью проводится интенсивная терапия, имеющая целью поддержание функций
жизненно важных органов и систем, и одновременно принимаются меры профилактики
дальнейшего травмирования спинного мозга.) Мы кратко остановимся на этих мероприятиях,
поскольку, хотя они и не являются непосредственно реабилитационными, но от их
своевременности и качественности во многом зависит дальнейший прогноз восстановления
функций.
Для предотвращения вторичных смещений в позвоночнике транспортировка пострадавших
с ПСМТ должна осуществляться только на щитах или на жестких носилках, в положении
больного на спине, при этом для иммобилизации поврежденного отдела позвоночника
применяются специальные шины. При перекладывании больного, при выполнении диагностических
исследований перемещение пациента должно производиться исключительно осторожно,
с исключением сгибания, разгибания, ротации и боковых смещений позвоночника.
К перемещению пациента должно быть привлечено не менее 4 человек обслуживающего
персонала.
Интенсивная терапия в остром периоде ПСМТ направлена на поддержание функции
жизненно важных органов. Обязательно поддержание артериального давления на уровне
нормальных значений. Гипотензия приводит к усугублению нарушений спинального
кровообращения в зоне повреждения. И только на этом фоне проводится лечение
отека спинного мозга: назначаются диуретики, обеспечивающие форсированный диурез
(фуросемид), уменьшающие образование цереброспинальной жидкости (диакарб), регулирующие
электролитный обмен (верошпирон). В последние годы доказано особое значение
высоких доз метилпреднизолона в остром периоде ПСМТ. Препарат Солу-Медрол (Solu-medrol,
англ., водорастворимая соль метилпреднизолона) вводится из расчета 30 мг/кг
в первые 15 минут после поступления больного, а затем по 5,4 мг/кг/в час в течение
последующих 23 часов. В среднем, больной весом в 80 кг должен в первые 8 часов
после травмы получить 13 г метилпреднизолона. Эта тактика способствует более
полному восстановлению утерянных двигательных функций [Bracken М. и соавт.,
1992]. Действие метилпреднизо-лона заключается в том, что он ингибирует перекисное
окисление липидов, вызываемое свободными радикалами; поддерживает кровоснабжение
ткани спинного мозга и аэробный энергетический метаболизм; усиливает возбудимость
нейронов и проведение импульсов. Применение метилпреднизолона в высоких дозах
у больных с травмой спинного мозга в остром периоде в первые 8 часов после нее
названо достижением медицины.
Вводятся также реологически активные препараты, поддерживающие гематокрит на
уровне 33-35%, ноотропы. В первые 4-6 часов после травмы может быть эффективная
локальная гипотермия спинного мозга, которая проводится во время операции. При
травматическом шоке для поддержания объема циркулирующей крови вводят низко-
и высокомолекулярные декстраны, плазму, кровь в объеме до 800-1200 мл. Нельзя
допускать гиповолемии, усугубляющей расстройства кровообращения, поэтому больной
должен получать не менее 2.5 л жидкости в день, и столько же выделять. При развитии
острой дыхательной недостаточности (паралич дыхательной мускулатуры либо восходящий
отек спинного мозга) показана вспомогательная вентиляция легких либо искусственная
вентиляция газовой смесью в режимах умеренной гипервентиляции. При присоединении
пневмонии вентиляцию проводят с положительным давлением в конце выдоха [Гайдар
Б.В. и соавт., 1997]. При отсутствии тяжелых повреждений спинного мозга, а также
нарушений сознания и гемодинамики искусственная вентиляция легких проводится
через интубационную трубку, предпочтителен назотрахеальный метод интубации.
В остальных случаях, в особенности при необходимости длительной искусственной
вентиляции у больных с тяжелой травмой шейного отдела спинного мозга, накладывается
трахеостома. Следует помнить, что интубация больных с травмой шейных позвонков
через естественные отверстия противопоказана из-за возможности вторичного смещения
позвонков. При определении показаний к трахеостомии наряду со степенью острой
дыхательной недостаточности учитывают клинические особенности спинальной травмы
[Гайдар Б.В., 1997]:
- трахеостомия не показана, как правило, при незначительном и умеренном нарушениях
проводимости шейного отдела спинного мозга;
- трахеостомия показана при полном и значительном нарушениях проводимости спинного
мозга при травмах С1-С5 позвонков (операция проводится при поступлении в стационар);
- трахеостомия показана при полном и частичном нарушениях проводимости при
травмах VI шейного позвонка лишь при возникновении признаков острой дыхательной
недостаточности (операция чаще проводится на 3-7 день после травмы);
- при травмах С7-Тh12 позвонков трахеостомия показана при полном и значительном
частичном нарушениях проводимости спинного мозга и неэффективности консервативных
мер по устранению острой дыхательной недостаточности, особенно осложняющей двухстороннюю
пневмонию.
При высокой тетраплегии осуществляют электростимуляцию диафрагмы. Проводят
также поддержание сердечной деятельности (сердечные гликозиды, антагонисты кальция,
оксигенотерапия, вазоактивные средства), коррекцию метаболических нарушений
и поддержание электролитного баланса. Больным с травмой спинного мозга в обязательном
порядке с первых дней назначают антибактериальную терапию, используя сразу антибиотики
широкого спектра действия либо подбирая их с учетом чувствительности антифлоры.
Осуществляется 4-х разовая периодическая катетеризация мочевого пузыря с промыванием
его дважды в день раствором фурациллина в разведении 1:5000 (а при наличии уроинфекции
- раствором фурациллина с антибиотиками, чувствительными к патогенной флоре),
либо подключается система Монро.
При открытой ПСМТ производится первичная хирургическая обработка раны,
при наличии ликвореи - ламинэктомия с ушиванием или пластическим закрытием раны
твердой мозговой оболочки.
Показания к оперативному вмешательству возникают также при компрессии
спинного мозга и его магистральных сосудов, либо при реальной угрозе такой компрессии
(абсолютная нестабильность позвоночника). Все операции при ПСМТ разделяют на
три типа: декомпрессивные, стабилизирующие, дакомпрессивно-стабилизирующие.
Декомпрессивные операции проводят по следующим показаниям [Луцик А.А., 1994]:
1. выраженная деформация позвоночного канала рентгенонегативными или рентгенопозитивными
компрессирующими структурами;
2. частичный или полный блок ликворных путей;
3. прогрессирование дисфункции спинного мозга;
4. прогрессирование вторичной острой дыхательной недостаточности вследствие
восходящего отека поврежденного шейного отдела спинного мозга;
5. клинические и ангиографические признаки сдавления магистрального сосуда
спинного мозга.
Неустраненное в первые 6 часов после травмы сдавление спинного мозга вызывает
в нем изменения, которые на 80% необратимы. Поэтому декомпрессия спинного мозга
должна производиться в максимально короткие сроки после травмы (первые 4-6 часов),
до наступления в спинном мозге необратимых постишемических расстройств. К возможным
противопоказаниям к декомпрессии относятся: травматический шок, сопутствующие
повреждения внутренних органов, ранние септические осложнения ПСМТ, острая дыхательная
и другая бульбарная недостаточность. Эти противопоказания должны быть ликвидированы
как можно быстрее, иногда допускается проведение противошоковых мероприятий,
восстановление целостности внутренних органов и пр. параллельно с декомпрессией
мозга. В ряде случаев декомпрессия спинного мозга производится бескровно (вправление
вывихов шейных позвонков, одномоментное закрытое либо путем вытяжения; реклинация
и репозиция сломанных позвонков в области грудо-поясничного перехода). Декомпрессия
обязательно завершается стабилизацией позвоночника. Различают внешнюю стабилизацию
(корсеты, шины, вытяжение) и внутреннюю (хирургические методы). Характер мероприятий
по стабилизации позвоночника и декомпрессии (либо предотвращению компрессии)
спинного мозга в зависимости от вида травмы позвоночника отражен в таблице
9.2.
Таблица 9.2. МЕРОПРИЯТИЯ ПО СТАБИЛИЗАЦИИ ПОЗВОНОЧНИКА И
ДЕКОМПРЕССИИ СПИННОГО МОЗГА ПРИ РАЗЛИЧНЫХ ТРАВМАХ ПОЗВОНОЧНИКА
(по О.А. Перльмуттер, 2000; Я.Л.Цивьяну, 1993)
Вид травмы |
Характер и продолжительность стабилизирующих мероприятий |
| 1.Стабильные повреждения шейного
отдела позвоночника |
| Ушиб позвоночника |
Воротник Шанца на 5-7 дней. |
| Капсульно-связочные повреждения |
Ватно-марлевый воротник Шанца сроком на 2-3 недели. |
| Перелом зубовидного отростка II или III типов без смещения |
Кранио-торакальная гипсовая повязка или конструкция типа
Halo на 4-8 мес. Атланто-аксиальный или окципитоспондилодез с помощью конструкций
типа системы Apofix. |
| Стабильный перелом дужек аксиса |
Краниоторакальная гипсовая повязка до 6 мес. Интраламинарная
фиксация С1-3 с помощью конструкций типа Apofix, Medbioteh и др. |
| Сгибательный подвывих С3-С7 позвонков |
В свежих случаях - одномоментное ручное вправление по Гютеру,
либо вытяжение петлей Глиссона с последующей иммобилизацией мягким или гипсовым
воротником Шанца на 2-4 недели, при повреждении связочного аппарата -до
8-10 недель. |
| Разгибательное стабильное повреждение С3-С7 позвонков (незначительный
антелистез) |
Гипсовая краниоторакальная повязка или воротник Шанца с высоким
передним и задним козырьком на 3-6 месяца, либо (при более выраженном смещении)
- ручное вправление или скелетное вытяжение за кости черепа, или галотракция
с последующей иммобилизацией кранио-торакальной повязкой. |
| Стабильные взрывные переломы тел позвонков (при незначительном
снижении высоты тела позвонка) |
Гипсовая краниоторакальная повязка или лечение в аппарате
типа Halo сроком на 3 месяца. |
2. Нестабильные повреждения шейного отдела позвоночника |
| Атланто-окципитальный вывих |
Вправление и иммобилизация с помощью скелетного вытяжения
или галотракции с последующей длительной иммобилизацией краниоторакальным
гипсовым корсетом. Оперативное лечение - атланто-окципитальный спондилодез
с последующей длительной иммобилизацией краниоторакальным гипсовым корсетом.
Сроки иммобилизации - 4-6 мес. |
| Лопающийся перелом Джефферсона |
Репозиция отломков и иммобилизация с помощью скелетного вытяжения
за кости свода черепа с грузом в 4,5 кг, затем перевод в краниоторакальную
гипсовую повязку сроком на 12 мес, либо лечение в аппарате Halo. Первичное
наложение краниоторакальной повязки на срок до 1 года. |
| Передний ротационный подвывих атланта |
Одномоментное ручное вправление по Гютеру, деротационное
вытяжение или вытяжение на петле Глиссона в течение 1 суток с последующей
иммобилизаций ватно-марлевым воротником Шанца на 2-3 суток. |
| Трансдентальный вывих атланта |
Разнообразные виды атланто-аксиального спондилодеза (доступами
спереди или сзади) с иммобилизацией кранио-торакальной гипсовой повязкой
в течение 3-4 месяцев до формирования костного сращения. Репозиция с помощью
скелетного вытяжения или в аппарате Halo. Иммобилизация не менее 6 месяцев. |
| Застарелый трансдентальный вывих антланта |
Двухэтапное вмешательство:
- задняя декомпрессия спинного мозга, включающая резекцию дуги атланта и
заднего края большого затылочного отверстия, заканчивающаяся окципитоспондилодезом;
- передняя декомпрессия спинного мозга доступом Fang et Ong. возможен передний
спондилодез между передним краем затылочной кости и телом С2. Иммобилизация
в торакокраниальной гипсовой повязке сроком на 4-6 мес. |
| Транслигаментозный вывих атланта |
Вправление с помощью скелетного вытяжения за кости свода
черепа в течение 6 недель, затем перевод в торакокраниальную гипсовую повязку
сроком на 4-6 месяцев.
Трансартикулярная атланто-аксиальная фиксация с помощью винтов, задний спондилодез
аутостружкой с последующей иммобилизацией торакокраниальной повязкой сроком
на 3-4 месяца. |
| Нестабильный перелом дужек аксиса |
Передний спондилодез С2-С3 с последующей галотракцией
в течение 4-6 недель, и наложение краниоторакальной гипсовой повязки до
образования костного блока. |
| Сгибательные вывихи С3-С7 позвонков |
При свежих вывихах
Одномоментное ручное вправление способом Рише-Гютера с последующим удерживающим
вытяжением (груз 4-6 кг) на петле Глиссона в течение 3-6 недель, затем перевод
в гипсовую краниоторакальную или цервикоторакапьную повязку сроком до 2,5
мес. с обязательным рентгеноконтролем на каждом этапе.
Вправление вывихов с помощью форсированного вытяжения за кости черепа большими
грузами в течение суток, затем удерживающее вытяжение на петле Глиссона
в течение 3-6 недель и перевод в гипсовую краниоторакальную или цервикоторакальную
повязку сроком до 2,5 мес. с обязательным рентгеноконтролем на каждом этапе.
Грузы рассчитываются исходя из того, что на голову требуется 4,5 кг + дополнительно
на каждый вышерасположенный от поврежденного позвоночно-двигательный сегмент
по 2,3 кг. Применение гапоаппарата в течение всего срока или в первые 3-6
недель с последующим переводом в гипсовую повязку до 2,5-3 месяцев. Хирургическое
лечение - открытое вправление вывиха задним доступом с межостистым, интраламинарным,
межсуставным спондилодезом с последующей краниоторакальной гипсовой иммобилизацией
на 6-8 недель. Хирургическое лечение - передняя дискэктомия с попыткой вправления
вывиха и передний
спондилодез ауто- или аллотрансплантатом с последующим переводом больного
в гипсовую повязку на срок до 3 месяцев: при укреплении спондилодеза
фиксирующими пластинами сроки иммобилизации могут быть снижены до 2,5 мес.
При отсутствии результатов вправления и застарелых вывихах
Передняя орпорэктомия вместе со смежными дисками и передний спондилодез
ауто-, аллотрансплантатом с последующей иммобилизацией гипсовой повязкой
до 3-4 мес; при дополнительном укреплении спондилодеза с помощью фиксирующих
пластин - 3 мес. |
| Нестабильные взрывные переломы тел позвонков без деформации
позвоночного канала и компрессии спинного мозга |
Скелетное вытяжение за кости свода черепа грузом, 6-8 кг
в течение 2-3 недель, затем иммобилизация краниоторакальной гипсовой повязкой
на 3-4 месяца; либо оперативное лечение, завершающееся спондилодезом, а
через 7-10 суток - иммобилизация краниоторакальной гипсовой повязкой. |
| Нестабильные взрывные переломы тел позвонков с деформацией
позвоночного канала и компрессией спинного мозга |
Передняя корпорэктомия вместе со смежными дисками и передний
спондилодез ауто- или аллотранплантатами, возможно с дополнительной фиксацией
блокирующими пластинами с последующим переводом в гипсовую повязку сроком
на 3-4 месяца. |
| Нестабильные сгибательные и разгибательные повреждения С3-С7
позвонков без компрессии спинного мозга |
Передний спондилодез, с дополнительным укреплением его блокирующей
пластиной типа Mathys, затем после снятия швов - перевод в гипсовую повязку
сроком на 3 мес. |
| Нестабильные сгибательные и разгибательные повреждения С3-С7
позвонков с компрессией спинного мозга |
Передняя декомпрессия спинного мозга и его корешков, завершающаяся
передним спондилодезом, возможно, с дополнительным применением блокирующих
пластин типа Mathys, затем, после снятия швов - перевод в гипсовую повязку
сроком на 3 месяца. |
| 3. Повреждения грудных и поясничных
позвонков |
| Ушибы позвоночника |
Постельный режим 7-14 дней. |
| Изолированные разрывы межостистой связки, изолированные переломы
остистых, поперечных и суставных отростков |
Иммобилизации не требуют (постельный режим 1-2 недели). |
| Изолированные разрывы надостистой связки |
Иммобилизация в течение 4-6 недель задней гипсовой
кроваткой или гипсовым корсетом в положении умеренного разгибания поясничного
отдела позвоночника. При выраженных болях - оперативное лечение, заключающееся
в сшивании связки, иммобилизация с теми же сроками. Транспедикулярная фиксация,
перевод в вертикальное положение через 3 недели. К труду через 3 месяца. |
Переломы типа А1 и А2 (компрессионные,
компрсссионно-оскольчатые)
без повреждения задних отделов
тела позвонка |
Одномоментная репозиция в течение первых 7 дней гипсовым
корсетом на 3-6 мес. Функциональный метод Гориневской-Древинг (укрепление
мышечного
корсета путем лечебной гимнастики) в течение 2 2.5 месяцев. При компрессии
более чем на 1/3 в первые 7 дней репозиция перелома с помощью транспедикулярных
конструкций. |
| Переломы типа А3 (взрывные переломы тел) без деформации позвоночного канала
и сдавления спинного мозга |
Одномоментное форсированное вправление с последующей иммобилизацией большим
гипсовым корсетом на 3-4 месяца по Холдсворду, 9-12 месяцев по Каплану.
Оперативное вмешательство только на теле позвонка, заканчивающееся передним
спондилодезом боковым или переднебоковым доступами с дополнительным укреплением
спондилодеза конструкциями типа VenroFix или Z-plate. Постельный режим в
течение 4-6 нед. Иммобилизация производится до наступления выраженного вентрального
костного блока. В первые 7 дней после травмы возможна репозиция перелома
с помощью транспедикулярных фиксаторов, подъем больных разрешается через
4-6 недель. Наложение корсета до 6 месяцев недисциплинированным пациентам
и людям, выписанным на работу. |
| Переломы типа А3 с деформацией позвоночного канала и сдавлением спинного
мозга |
Оперативное вмешательство только на теле позвонка - передняя декомпрессия
спинного мозга, заканчивающаяся передним спондилодезом боковым или переднебоковым
доступами с дополнительным укреплением спондилодеза конструкциями типа VenroFix
или Z-plate. Послеоперационный постельный режим в течение 4-6 недель, затем
больного поднимают на ноги. Корсет до наступления выраженного вентрального
костного блока накладывается больным, выполняющим тяжелый физический труд
и недисциплинированным. |
| Переломы типа В без компрессии спинного мозга |
Оперативное лечение с помощью транспедикулярных конструкций, позволяющих
восстановить правильную ось позвоночного канала. Перевод в вертикальное
положение через 6 недель, гипсовый корсет (до года) при тяжелой работе или
недисциплинированности больного. |
| Переломы типа В с передней компрессией спинного мозга или корешков конского
хвоста |
Двухэтапное вмешательство - передняя декомпрессия спинного мозга и корешков
конского хвоста, заканчивающаяся породним спондилодезом. Вторым этапом -
транспедикулярная фиксация. Перевод в вертикальное положение - через 6 недель,
наложение гипсового корсета (до года) при тяжелой работе или недисциплинированным
больным.
|
| Переломы типа С |
При неосложненных переломах в первые/дней после травмы возможна репозиция
перелома с помощью транспедикулярных фиксаторов с дополнительным укреплением
их поперечной стяжкой с теми же рекомендациями по постельному режиму и наложению
корсета, что и переломы типа В. При сдавлении спинного мозга или корешков
конского хвоста - поэтапная декомпрессия этих образований, передний спондилодез
и транследикулярная фиксация с укрепляющими дополнениями с теми же рекомендациями
по постельному режиму и наложению корсета. |
В настоящее время техника оперативных вмешательств совершенствуется, появляются
все более и более современные фиксирующие материалы и устройства. В настоящее
время наиболее перспективным и наилучшим способом фиксации поврежденного позвоночно-двигательного
сегмента считается транспедикулярная фиксация, в некоторых случаях в комбинации
со спондилодезом. Этот вид лечения ПСМТ восстанавливает правильную ось позвоночника,
существенно сокращает сроки постельного режима, способствует более ранней активизации
больных и расширяет реабилитационные возможности.
Необходимо отметить, что адекватное хирургическое лечение, направленное на
всестороннюю декомпрессию спинного мозга, восстановление циркуляции ликвора
и целостности твердой мозговой оболочки, стабилизацию дестабилизированного отдела
позвоночника, является основой успеха дальнейших реабилитационных мероприятий.
В случаях, когда такое хирургическое вмешательство не было осуществлено своевременно
(в ранние сроки), его необходимо выполнить в любые сроки после травмы.
9.2.2. Ранний период
В раннем периоде ПСМТ реабилитологом решаются следующие задачи: предупреждение
и лечение пролежней, контрактур, болей, атрофии мышц и прочих осложнений ПСМТ;
лечение нарушений функции тазовых органов; создание максимально благоприятных
условий для течения восстановительных процессов в спинном мозге.
9.2.2.1. Уход за больным
Первоочередное внимание уделяется обеспечению правильного ухода за больным,
что позволяет предупредить развитие пролежней и контрактур.
Профилактика пролежней заключается в гигиеническом содержании постели,
щадящем дозированном переворачивании, наблюдении за состоянием кожных покровов
и протирании кожи камфорным или салициловым спиртом, подкладыванием под пятки,
крестец и другие костные выступы поролоновых или резиновых кругов, использование
мягких матрасов из пористой резины или специальных противопролежневых матрасов.
При травмах грудного и поясничного отделов позвоночника целесообразно положение
больного "на животе", шейного - "на спине". В лечении пролежней
в зависимости от стадии процесса используют различные мазевые повязки, стимулирующие
регенерацию препараты, УВЧ, ультрафиолетовое облучение, аутодермопластику или
пластику перемещенным лоскутом и т.д. (глава
5.2).
Профилактика контрактур заключается в правильной укладке конечности,
в том числе с помощью специальных лонгет и ортезов, в проведении массажа и лечебной
гимнастики (глава 5.1).
Профилактика тромбоза глубоких вен проводится путем бинтования ног эластичными
бинтами и назначения низких доз гепарина, при развившемся тромбозе глубоких
вен назначают гепарин внутривенно в адекватных дозировках под контролем АЧТВ
с постепенным переходом на варфарин под контролем протромбинового индекса (глава
5.4).
9.2.2.2. Лечение нарушений функций тазовых органов
К важнейшим задачам относятся восстановление пассажа мочи и резервуарно-выделительной
функции мочевого пузыря (восстановление пузырного рефлекса), профилактика и
лечение уроинфекции.
При стойкой задержке мочеиспускания для выведения мочи применяют либо
периодическую катетеризацию мочевого пузыря, либо приливно-отливный дренаж (систему
Монро). Катетеризация мочевого пузыря проводится 4-6 раз в день. Поскольку
эта манипуляция связана с большим риском инфицирования мочевыводящих путей (вплоть
до уросепсиса), она должна сопровождаться строжайшим выполнением правил асептики
и антисептики. Обязательна обработка кожи и слизистой вокруг мочеиспускательного
канала - например, водным раствором хлоргексидина. Катетер должен быть стерильным,
его смазывают антимикробной мазью (левомиколь, дибунол). Диаметр катетера должен
быть меньше диаметра уретры, вводить катетер следует без усилий, оставлять в
уретре и мочевом пузыре. Частота катеризации подбирается такая, чтобы не допускать
скопления мочи в пузыре более 350 мл (обычно - не реже 3 раз в сутки). Периодическая
катетеризация, в отличие от постоянной, сопряжена с меньшим риском развития
пролежней, камней, инфекционных осложнений в мочевыводящих путях [Guttman L.,
Frankel М. и соавт., 1966]. Параллельно с катетеризации осуществляются мероприятия
по профилактике уроинфекции. В зависимости от выраженности воспалительных явлений
ежесуточно, через сутки или 1-2 раза в неделю производят промывание мочевого
пузыря фурациллином с добавлением диоксидина и уросептиков (фурагин, фурадонин,
5-НОК, невиграмон и др.). При асимптомной бактериурии не рекомендуют вводить
антибиотики во избежании развития резистентных штаммов [Stover S. и соавт.,
1989]. При возникновении клинических признаков инфекции (лихорадка, лейкоцитоз)
назначают антибиотики, выбор которых осуществляется после определения чувствительности
флоры к антибактериальным препаратам.
Приливно-отливная система Монро состоит из стерильного сосуда, заполненного
антисептической жидкостью (фурацилин 1:5000), закрытого сосуда для сбора мочи
и катетера, который с помощью тройника соединяется с вышеуказанными сосудами.
Скорость подачи жидкости в катетер регулируется с помощью регулятора частоты
капель. Сущность приливно-отливного дренирования мочевого пузыря заключается
в том, что антисептик редкими каплями (40-60 в мин.) поступает в мочевой пузырь.
Отводящее колено системы Монро устанавливают на высоту, необходимую для выработки
нормального тонуса детрузора. Поскольку оптимальным давлением в полости мочевого
пузыря, необходимым для выработки пузырного рефлекса, является давление 150
мм водного столба, то отводящий конец трубки поднимают обычно на 15 см выше
уровня мочевого пузыря. При достижении этого давления в мочевом пузыре моча
начинает механически вымываться из мочевого пузыря вместе с фурацилином. С учетом
данных цистометрии и сфинктерометрии эта высота колена может быть отрегулирована.
Так, при гипотонии детрузора отводящее колено рекомендуют устанавливать на высоте
не более 5- 7 см над тройником, а при резко выраженной гипертонии колено поднимают
до 25-30 см [Потемкин И.М., 1994].
Преимущества системы Монро в сравнении с периодической катетеризацией заключаются
в том, что отпадает необходимость несколько раз в сутки заводить катетер в мочевой
пузырь; мочевой пузырь всегда содержит антисептическую жидкость, что препятствует
сморщиванию его стенок и предотвращает развитие цистита и восходящей инфекции;
объем жидкости, содержащийся в мочевом пузыре под давлением 150 мм вод. ст.,
адекватно раздражает стенку, вызывая ее рефлекторное сокращение и способствуя
выработке пузырного рефлекса. Однако эти преимущества имеют место лишь в случае
правильного применения системы: катетер должен быть точно подобран по диаметру
уретры (более тонкий способствует мочевым затекам, а более толстый - пролежням
уретры); через каждые 7 дней систему Монро отключают, переводя больного на три
дня на периодическую катетеризацию. Противопоказанием к установке системы Монро
служат воспаление или повреждение уретры и ли наружных половых органов, когда
постоянный катетер использовать нельзя.
Выбор методики выведения мочи зависит от прогноза скорости восстановления функций
тазовых органов: периодическую катетеризацию применяют в случаях частичного
нарушения проводимости спинного мозга, когда есть надежда на быстрое восстановление
рефлекторного или произвольного мочеиспускания, а систему Монро - при более
грубых нарушениях, требующих длительного времени для выработки рефлекторного
мочеиспускания.
Восстановление пузырного рефлекса с повышением внутрипузырного давления до
800-900 мм водн. ст., являющимся нормальным пузырным давлением во время акта
мочеиспускания, свидетельствует о том, что рефлекторный аппарат мочевого пузыря
способен действовать в произвольном или автоматическом режиме, и пора прекращать
дренирование мочевого пузыря. Дренирование мочевого пузыря прекращают при восстановлении
самостоятельного мочеиспускания с объемом остаточной мочи менее 50 мл.
Эпицистостомию в настоящее время производят только при невозможности
проведения катетера по уретре: разрыв, пролежни, стриктуры уретры, аденома предстательной
железы и т.д. Эпистостома должна быть закрыта в максимально ранние сроки, как
только будут ликвидированы противопоказания для установки приливно-отливного
дренажа. Такой подход обусловлен тем, что эпицистостомия способствует развитию
уросептических осложнений, которые рано или поздно развиваются у всех больных
с надлобковым свищем, а также приводит к формированию "сморщенного"
мочевого пузыря [Бабиченко Е.И., 1994].
Для восстановления нормальной функции мочевого пузыря, помимо его дренирования,
уже в раннем периоде начинают использовать физиотерапию и иглорефлексотерапию,
ограничиваясь теми методиками, которые можно проводить в палате, без дополнительных
перевозок больного в физиотерапевтические кабинеты; более подробно аспекты физиотерапии
нарушений тазовых функций будут рассмотрены в разделе 9.3 (все физиотерапевтические
процедуры назначают с учетом состояния сердечно-сосудистой системы, по мере
стабилизации состояния жизненно-важных функций).
9.2.2.3. Стимуляция восстановительных процессов в спинном мозге
С этой целью применяют медикаментозную терапию, физиотерапию, лечебную гимнастику,
иглорефлексотерапию.
Из медикаментозных средств используют препараты, нормализующие
обмен веществ, улучшающие капиллярный кровоток и снабжение спинного мозга кислородом,
стимулирующие проводимость, повышающие реактивность, снижающие активность гиалуронидазы
и смягчающие развитие глиозной ткани:
- ноотропы (ноотропил 20% раствор по 5-10 мл ежедневно внутримышечно
или внутривенно, 25-30 инъекций на курс, либо по 1.2 г дважды в день перорально
в течение месяца);
- витамины (тиамин, пиридоксин, цианокобаламин, аскорбиновая кислота
в общепринятых дозировках);
- анаболические гормоны (ретаболил 5% по 1 мл внутримышечно 2-4 иньекции
в месяц);
- вазо- и реологически активные средства (кавинтон по 10 мг в сутки
внутривенно капельно, 10-15 вливаний, с последующим переходом на пероральный
прием по 5 мг трижды в день в течение месяца; агапурин, реополиглюкин, актовегин
и др.);
- иммуноактивные препараты (левамизол 150 мг внутрь через сутки, тималин
10 мг внутримышечно один раз в сутки, курс - в течение месяца);
- биогенные стимуляторы и ферменты (эктракт алоэ по 1 мл подкожно один
раз в сутки, румалон по 1 мл внутримышечно один раз в сутки, лидаза 64 ед
внутримышечно в 1мл 0.5% раствора новокаина 1 раз в сутки, курсы - в течение
месяца);
- миорелаксанты (при спастических параличах, см. главу
4);
- по показаниям - седативные и транквилизирующие препараты.
Физиотерапия предполагает использование одной или нескольких
(сочетающихся между собой) методик курсами до 20 процедур на курс, при условии
того, что имеется возможность проводить процедуры в палате:
- электрическое поле УВЧ поперечно на очаг поражения в нетепловой
или слаботепловой дозе, в непрерывном или импульсном режиме при малой выходной
мощности;
- УВЧ -индуктотермия на очаг поражения в олиготермической дозе;
- электрофорез лидазы в чередовании с иод-электрофорезом по поперечной
методике;
- продольная гальванизация с накладыванием электродов выше и ниже очага
поражения спинного мозга;
- аппликации грязи (при консервативном ведении - с начала 2-й недели
после травмы, при оперативном - после снятия швов с послеоперационной раны).
Проводят в положении на животе, либо, при повреждении шейного отдела - на
боку. Температура грязи 40-44°, при сердечнососудистых нарушениях - 36-38°.
При отсутствии сосудистых и дыхательных расстройств и удовлетворительном соматическом
состоянии применяют очагово-сегментарно-проводниковую методику и продолжительность
процедур 15-20 минут; при вегетативной лабильности, сердечно-сосудистых и
дыхательных осложнениях ограничиваются очаговой методикой с сокращением времени
процедур до 10-12 минут.
Лечебная гимнастика
Характер лечебной гимнастики в ранний период определяется в первую очередь
степенью повреждения спинного мозга и степенью стабильности повреждения позвоночника.
При отсутствии грубых нарушений функции спинного мозга и стабильном характере
перелома позвоночника кинезотерапия начинается сразу же после поступления
больного в стационар, при нестабильном характере повреждения позвоночника -
после выполнения стабилизирующих мероприятий, не нарушая режима иммобилизации
(т.е. во время занятий больной остается в гипсовой повязке, в воротнике, на
реклинаторе и т.д.). Задачей гимнастики является улучшение функции сердечнососудистой
и дыхательной систем, желудочно-кишечного тракта, общетонизирующее воздействие,
а также предупреждение атрофии мышц. Лечебную физкультуру назначают в форме
индивидуальных занятий.
В раннем периоде лечебную гимнастику начинают с дыхательных упражнений и упражнений
для дистальных отделов конечностей. Постепенно добавляют те движения, в которых
участвуют, мышцы, прикрепленные к позвоночнику, при сохранении неподвижности
самого позвоночника.
При травме шейного отдела позвоночника занятия проводят вначале в исходном положении
лежа на спине, к концу раннего периода - в положениях сидя и стоя.
Выполняют упражнения для дистальных отделов конечностей и дыхательные упражнения
(статические и динамические). Соотношение упражнений для конечностей и дыхательных
упражнений составляет в первые дни 1:2, в последующем 3:1, 4:1. Рекомендуют
так же движения нижней челюстью - широкое открывание рта, движения вправо, влево,
вперед. Все упражнения выполняют в медленном темпе с паузами для отдыха. Исключаются
упражнения в прогибании туловища, повороты и наклоны головы. Примерный комплекс
упражнений представлен в таблице 9.3.
Таблица 9.3. ПРИМЕРНЫЙ КОМПЛЕКС УПРАЖНЕНИЙ В РАННЕМ ПЕРИОДЕ
ТРАВМЫ ШЕЙНОГО ОТДЕЛА ПОЗВОНОЧНИКА (ПРИ ОТСУТСТВИИ ГРУБЫХ НАРУШЕНИЙ ФУНКЦИИ
СПИННОГО МОЗГА)
(по В.А. Епифанову, 1987)
Исходное положение |
Упражнения |
Методические указания |
| Лежа на спине |
Диафрагмальное дыхание.
Тыльное и подошвенное сгибание стоп.
Сжимание и разжимание пальцев кисти.
Круговые движения стопами.
Сгибание и разгибание рук в локтевых суставах.
Попеременное сгибание ног в коленных суставах, не отрывая
стопы от плоскости постели.
Диафрагмальное дыхание.
Сгибание и разгибание в лучезапястных суставах.
Попеременное отведение и приведение ног.
Круговые движения в лучезапястных суставах.
Диафрагмальное дыхание. |
Все упражнения выполняются по 4-5 раз в медленном темпе |
Кинезотерапия в остром и начале раннего периоде при травме грудного и поясничного
отделов позвоночника проводится в положении больного лежа на кровати на щите
с приподнятым головным концом кровати. Исходное положение - лежа на спине.
Используют дыхательные упражнения, упражнения мелких и средних мышечных групп
и суставов, активные движения ногами в облегченных условиях (использование
наклонной плоскости) и попеременно (таблица 9.4). Продолжительность
занятия составляет 5-7 минут. Кратность - 3-5 раз в день. К концу для раннего
периода, если позволяет иммобилизационный режим, лечебную гимнастику можно
выполнять из исходных положений на животе.
Таблица 9.4. ПРИМЕРНЫЙ КОМПЛЕКС УПРАЖНЕНИЙ ПРИ ТРАВМЕ
НИЖНЕГРУДНОГО И ПОЯСНИЧНОГО ОТДЕЛОВ ПОЗВОНОЧНИКА В РАННЕМ ПЕРИОДЕ (14-Й ДЕНЬ)
(по Т.Н.Кукушкиной и соавт., 1981)
Исходное положение - лежа на спине
1. Руки вдоль туловища ладонями вверх, тыльное сгибание в голеностопных
суставах и рук в локтевых суставах, пальцы сжаты в кулак (10-12 раз).
2. Руки вдоль туловища, согнуть одну ногу, скользя ступней по постели, возвратиться
в исходное положение (по 6-7 раз каждой ногой).
3. Руки вдоль туловища, поднимание и опускание прямых рук - вдох, выдох
(по 4-5 раз каждой рукой).
4. Отвести прямую ногу, слегка отрывая ее от постели, возвратиться в исходное
положение. Голеностопный сустав во время движения ногой находится в положении
тыльного сгибания ( по 4-6 раз каждой ногой).
5. Руки согнуты в локтях, ступни стоят на постели, поднимать и опускать
таз - вдох, выдох (4-5 раз).
6. Руки вдоль туловища ладонями вниз, ноги согнуты, ступни стоят на постели
(одна нога на носке, другая на - пятке). Одновременное опускание одной пятки
и поднимание другой, и наооборот (12-16 раз).
7. Руки согнуты в локтях, ноги вытянуты, прогнуться в грудной части позвоночника,
не поднимая таза, опираясь на локти, голову и плечи, и удержаться в этом
положении, затем опуститься (6-7 раз).
8. Руки к плечам, развести локти, соединив лопатки, - вдох, опустить - выдох
(6-8 раз).
9. Руки вдоль туловища, ладонями вниз. Поднять прямую ногу до угла 45° к
плоскости постели (стопа в положении тыльного сгибания), "написать"
в воздухе пяткой цифры от 1 до 3-5, вернуться в исходное положение, дыхание
равномерное (2-3 раза каждой ногой).
10. Глубокое дыхание (30 сек).
11. Поворот вниз лицом.
Исходное положение - лежа на животе
12. Руки вдоль туловища. Поочередное сгибание ног в коленных суставах с
одновременным тыльным сгибанием стоп ( по 10-12 раз каждой ногой).
13. Руки согнуты в локтевых суставах. Опираясь на кисти и предплечья, поднять
голову и плечи, удержаться в этом положении, затем опуститься (6-8 раз).
14. Руки вдоль туловища. Согнуть ногу в коленном суставе (стопа в положении
тыльного сгибания), поднять ее, выпрямляя коленный сустав, и поставить на
носок, расслабить все мышцы ноги (по 6-8 раз каждой ногой).
15. Руки к плечам. Приподнять плечи, голову и верхнюю часть туловища, соединив
лопатки, удержаться в этом положении, расслабив мышцы (5-6 раз).
16. Руки вдоль туловища. Приподнять прямую ногу назад, отвести в сторону.
Вернуться в исходное положение ( по 6-7 раз каждой ногой).
17. Поворот на спину.
Исходное положение - лежа на спине
18. Глубокое дыхание (30 сек).
19. Руки вдоль туловища. Поочередное сгибание рук в локтевом суставе с одновременным
тыльным сгибанием разноименной стопы, упражнение делать с усилием (12-16 раз).
20. Поднимать прямые руки вверх - вдох, опускание с расслаблением мышц в конце
движения - выдох (6-7 раз).
Некоторые специальные упражнения для статического напряжения
мышц спины
Исходное положение лежа на спине
21. Ноги согнуты в тазобедренных и коленных суставах, ступни стоят на постели,
руки в стороны, пальцы сжаты в кулак. Прогнуться в грудной части позвоночника,
не отрывая таза. Удерживаясь в этом положении, выполнить круговые движения
руками.
22. Руки вдоль туловища ладонями вниз, ноги выпрямлены. Прогнуться, приподнимая
таз с опорой на голову, руки и пятки. Удержаться в этом положении.
Исходное положение лежа на животе
23. Руки сзади, пальцы сцеплены в "замок". Прогнуться в грудном
отделе позвоночника, удержаться в этом положении.
24. Держась руками за края кровати, поднять прямую ногу назад (стопа в положении
тыльного сгибания), удержаться в этом положении.
25. Упражнение 24 повторить двумя ногами одновременно.
26. Руки к плечам, круговые движения в плечевых суставах, с одновременным
прогибом в позвоночнике.
27. Держась руками за края кровати, приподняв прямые ноги, иммитировать ногами
движения стиля "кроль".
28. Руки опущены с постели. Прогнуться назад, разведя руки в стороны, соединяя
лопатки, удержаться в этом положении.
Кинезотерапия при позвоночно-спинномозговой травме, сопровождающейся нарушением
функций спинного мозга, проводится в форме индивидуальной гимнастики в палате
и включает активные и пассивные движения, а также дыхательные упражнения.
Дыхательная гимнастика особенно актуальна при повреждении шейного отдела спинного мозга. Целью дыхательной гимнастики является увеличения газообмена
легких, укрепление мышц диафрагмы и других мышц, участвующих в акте дыхания.
Дыхательные упражнения выполняют в сочетании с ручным массажем грудной клетки.
Проводят статические дыхательные упражнения, уделяя особое внимание диафрагмальному
дыханию. Динамические дыхательные упражнения с движениями рук в полном объеме
в первые 8-10 суток после травмы или операции производить не рекомендуют во
избежании травмирования послеоперационной раны или спинного мозга [Кукушкина
Т.Н. и соавт., 1981]. При повреждениях на нижнегрудном и пояснично-крестцовом уровнях проводят статические и динамические дыхательные упражнения с движениями
рук в полном объеме. В остром периоде длительность занятий составляет 3-5
минут, упражнения выполняются с помощью инструктора. По мере улучшения общего
состояния больного постепенно комплекс гимнастики расширяют. Примеры дыхательных
упражнений при травме спинного мозга:
-
выполнение глубокого вдоха и выдоха по команде инструктора;
-
глубокий вдох с одновременным отведением рук при помощи методиста, затем
глубокий выдох с одновременным опусканием рук на переднюю поверхность
грудной клетки;
-
выполнение глубоких вдохов и выдохов по команде инструктора, с одновременным
надавливанием на переднюю брюшную стенку (с помощью рук инструктора или
мешочка с песком);
-
пациент откашливается с одновременным нажатием на брюшную стенку;
-
с помощью дыхания отклонять подвешенный на нитке к прикроватному оборудованию
шарик;
-
при помощи вдоха "прокачивание" жидкости в сообщающихся сосудах.
Целью проведения пассивной гимнастики является профилактика контрактур
в суставах конечностей, улучшение трофики мышц, обеспечение афферентной импульсации
от паретичных конечностей. Сначала проводят пассивные движения в суставах дистальных
отделов конечностей, затем - сложные пассивные упражнения, заключающиеся в одновременном
сгибании в нескольких суставах. Очень важно, чтобы больной мысленно помогал
инструктору выполнять каждое движение, всецело сосредотачиваясь на упражнении.
"Мысленные" упражнения необходимо делать с первых дней после травмы,
пока не забыт двигательный стереотип.
Активная гимнастика при полном поражении спинного мозга назначается
для мышц, иннервируемых сегментами спинного мозга выше очага поражения, при
частичном поражении - также и для мышц, иннервируемых сегментами спинного мозга
ниже очага поражения. Используют изометрические упражнения, активные движения
в суставах конечностей. Продолжительность занятия составляет 10-15 минут. Нагрузку
строго дозируют, чтобы не допустить переутомления больного.
Иглорефлексотерапия (раздел написан А.Г.Поляковой)
К основным принципам использования иглорефлексотерапии при позвоночно-спинномозговой
травме относятся следующие [Цогоев А.С., Качан А.Т., 1996]:
- раннее включение ИРГ в комплекс реабилитационных мероприятий,
- обязательное воздействие на точки, расположенные в зоне иннервации уровня
поражения спинного мозга на заднем срединном канале и канале мочевого пузыря
(при этом необходимо учитывать дистантные нарушения, которые могут быть на значительном
расстоянии от места травмы);
- точки неспецифического действия, используемые при двигательных и чувствительных
нарушениях, находящиеся на наружных акупунктурных каналах, при пальпации определяются
по максимальной болезненности,
- точки патогенетического действия, находящиеся на внутренних акупун-ктурных
каналах, для того, чтобы уменьшить в них болевые ощущения или при неудобном
положении больного, можно раздражать через точки наружных акупунктурных каналов
(например, МС.6 через ТR.5; RР.9 через VВ.34);
- чтобы избежать болевых ощущений, которые могут спровоцировать ухудшение, необходимо
пользоваться приемами "ишемизации" тканей:
вводить иглу после точечного массажа или через проводник;
- следует избегать введение игл из золота или других высокоактивных металлов,
учитывая повышенную возбудимость мышц.
В остром периоде воздействуют на точки, находящиеся на уровне травмированного
сегмента спинного мозга (т.е. в шейном отделе на один, в верхнегрудном - на
два, в нижнегрудном - на три позвонка выше того, который по нумерации соответствует
поврежденному сегменту). Используются точки как по XIII (Т) меридиану, так и
по ходу VII(V) меридиана, то есть паравертебрально, что позволяет оказывать
воздействие на симпатический пограничный ствол вблизи очага [Шапкин В. И., Бусаков
С.С., Одинак М.М., 1987]. Многие авторы рекомендуют выше очага применять возбуждающий,
а ниже очага - тормозной метод. При состояниях с выраженными явлениями спинального
автоматизма целесообразнее применять местное воздействие на сегментарные точки
иглотерапией и точечный массаж тормозным методом на точки, располагающиеся по
передней поверхности бёдер и задней поверхности голеней. В рецептуру включают
точки ушной раковины АТ-55 (точка центральной нервной системы), 25 (ствол мозга),
108 (средний отдел спины) и другие точки соответствующего отдела позвоночника.
Для предупреждения и лечения пролежней иногда оказывается эффективным воздействие
на область третьего грудного сегмента [Огнев В.В., 1958], что соответствует
точкам я-мэнь XIII (Т) - 15, тао-дао XIII (Т) - 13, да-чжу VII (V) - 11.
Психотерапия
Повреждение спинного мозга является мощной стрессовой ситуацией, неизбежно
приводящей к кардинальным изменениям во всех сферах в жизни. Нежелание верить
в необратимость возникших изменений часто сменяется глубокой депрессией и пассивностью
больного, что затрудняет осуществление реабилитационных гцюграмм. До 50% больных
после ПСМТ начинают злоупотреблять алкоголем [Heinemann А. и соавт., 1988].
Психологическая адаптация к новым условиям существования длится иногда несколько
лет. Психотерапевтическая работа с больным должна начинаться с раннего реабилитационного
периода. Психолог и психотерапевт не только оказывают помощь больному, но и
консультируют членов реабилитационной бригады, родственников и членов семьи
пациента. Основными задачей психологической реабилитации становятся [Коган О.Г.,
Найдин В.Л., 1988]: достижение понимания больным реальных перспектив восстановления
утраченных функций; мобилизация воли больного для активного участия в реабилитационном
процессе; помощь в осознании больным необходимости и возможности социально полезной
трудовой деятельности и сохранения семьи даже при наличии стойких нарушений
функций и ограничений способности самостоятельного передвижения. Методы психотерапии
и формы проведения занятий выбираются индивидуально с учетом особенностей психического
состояния больного и реальных возможностей реабилитационного учреждения.
9.2.3. Современные подходы к решению проблемы восстановления функций при
повреждении спинного мозга
Поиск новых путей ускорения восстановления функций при ПСМТ продолжается непрерывно.
В последние годы в эксперименте особенно активно разрабатываются три стратегических
направления, касающиеся биологических вмешательств в процессы, происходящие
в поврежденном спинном мозге:
нейропротекция, содействие аксональной регенерации, активизация центров спинного
мозга, локализованных ниже уровня поражения (таблица 9.5).
Таблица 9.5. ТЕРАПЕВТИЧЕСКИЕ СТРАТЕГИИ, НАПРАВЛЕННЫЕ НА
УСКОРЕНИЕ ВОССТАНОВЛЕНИЯ ФУНКЦИЙ ПРИ ПОВРЕЖДЕНИИ СПИННОГО МОЗГА
(по М. Ribotta, А. Privat, 1999)
Нейропротекция
Антогонизм возбуждающим аминокислотам.
Защита от свободных радикалов.
Использование трофических факторов.
Аксональная регенерция
Предупреждение глиальных реакций, приводящих к образованию рубцов.
Блокирование ингибиторов регенерации.
Обеспечение адекватной трофической поддержки процессу регенерации поврежденных
аксонов.
Активизация центров спинного мозга, локализованных ниже уровня поражения
Сенсорномоторная стимуляция.
Поддержание супраспинальной афферентации: фармакотерапия, трансплантация, генная
терапия.
Нейропротекция предполагает использование определенных фармакологических
препаратов с целью затормаживания вторичных патологических процессов, развивающихся
в течение первой недели после первичной травмы спинного мозга. Напомним, что
обычно вслед за первичным повреждением ткани спинного мозга наблюдается реактивный
каскад патобиохимических реакций, приводящий к вторичному повреждению спинальных
нейронов: происходят патологические изменения в системе эндогенных трансмиттеров,
наблюдается усиленное образование свободных радикалов, происходит высвобождение
факторов, связанных с воспалением (цитокинов).
Среди эндогенных нейротрансмиттеров роль медиаторов клеточной смерти отводится
в первую очередь аминокислотам глутамату и аспартату, в норме обеспечивающим
процессы возбуждения. При повреждении спинного мозга происходит повышение уровня
этих эксайдотоксических аминокислот вне клетки. Глутамат активизирует постсинаптические
комплексы рецептор/канал, способствуя входу ионов Са2+ в клетку;
чрезмерное нерегулируемое поступление этих ионов в цитоплазму приводит к повреждению
клетки. Существует пять подтипов рецепторов, активизируемых глутаматом, среди
них в спинном мозге основным подтипом, участвующим в реализации нейротоксических
процессов, является подтип NMDA (N-метил-D-аспартат рецепторы). Блокирование
этих рецепторов препятствует открытию соответствующего канала для ионов кальция,
и может, видимо, в определенной степени защитить нейроны спинного мозга от вторичного
повреждения. На этом основана стратегия создания NMDA-антагонистов - фармакологических
препаратов, молекулы которых конкурируют с глутаматом во взаимодействии с NMDA-рецепторами
и таким образом оказывают нейропротективное действие [Mukhin A. и соавт., 1997].
Другим направлением нейропротекции является защита спинного мозга от повреждающего
действия свободных радикалов - использование антиоксидантов, препаратов, метаболизирующих
свободные радикалы, ингибирующих перекисное окисление липидов и т.д. Так, нейропротективный
эффект применения высоких доз метилпреднизолона связывают в первую очередь именно
с ингибированием перекисного окисления липидов. В эксперименте продолжается
создание новых препаратов с указанным механизмом действия. Изучаются также возможности
вмешательств в механизмы воспалительных процессов, развивающихся при спинномозговой
травме и способствующих вторичному повреждению спинного мозга [Carlson S. и
соавт., 1998].
Наконец, исследуются нейропротективные свойства трофических факторов - например,
в эксперименте показано, что факторы роста фибробластов 1 и 2 способствуют уменьшению
токсичности эксайторных аминокислот по отношению к мотонейронам спинного мозга;
возможно, целесообразно эти трофические факторы вводить локально в область травмы
либо способствовать их выработке в организме путем генной терапии [Teng Y. и
соавт., 1998].
Содействие аксональной регенерации - следующая стратегия, направленная
на устранение препятствий на пути регенерации аксона и на ускорение этой регенерации.
Росту аксона после спинномозговой травмы могут препятствовать следующие факторы
[М.Ribotta, А.Privat., 1999]:
1) быстрое образование глиального рубца в области повреждения спинного мозга;
2) наличие в тканях спинного мозга ингибиторов аксональной регенерации - таких,
как посттравматические компоненты экстрацеллюлярного матрикса, адгезивные молекулы,
связанные с миелином протеины;
3) недостаточное количество нейротрофных факторов и отсутствие субстратов, стимулирующих
рост аксонов.
Воздействия на глиальную рубцовую ткань с целью предупреждения гипертрофии
и гиперплазии в эксперименте проводятся путем рентгеновского облучения, а также
путем введения фармакологических препаратов (например, интрактектальное назначение
дериватов гидрохолестерола); результаты, полученные на животных, обнадеживают
[Vanek Р. и соавт., 1998; Рrivat А. и соавт., 1997].
В экспериментальных моделях продемонстрирована ингибирующая роль миелина на
регенерацию аксонов: так, после дискретной аксонотомии дорсальных канатиков
электронная микроскопия показала, что конусы роста присутствовали лишь в демиелинизированных
участках [Kierstead Н. и соавт., 1998]. Для нейтрализации ингибирующего эффекта
миелина делаются попытки использовать моноклональные антитела к протеинам олигодендроцитов.
Стимулирование роста аксонов и "перекидывание проводящего мостика"
через зону повреждения спинного мозга пытаются осуществить в эксперименте путем
трансплантации клеток или иных материалов - например, фрагментов периферических
нервов, при этом продемонстрирована способность аксонов нейронов спинного мозга
к регенерации [Chen D., и соавт., 1997]. Показано, что выраженным стимулирующим
эффектом обладают макрофаги, которые способствуют выработке фактора роста различными
клетками спинного мозга и создают благоприятные условия для аксональной регенерации
в области повреждения. Имеются также предварительные данные о положительных
результатах трансплантации шванновских клеток [Ramon-Сueto А., Аvila J., 1998],
эмбриональных клеток спинного мозга [Denier Р., Bregman В., 1998]. Многообещающей
является также генная терапия - трансплантация клеток, запрограммированных на
выработку факторов аксонального роста. Таким образом, к настоящему времени в
экспериментах на млекопитающих доказана способность многих нейронов спинного
мозга к регенерации, продолжаются поиски оптимальных условий для этой регенерации.
И, наконец, третье важнейшее стратегическое направление исследований касается активизации спинальных центров ниже уровня поражения. Эта стратегия предполагает
реорганизацию неповрежденных нервных связей и путей, которая теоретически возможна
в силу значительной пластичности нервной системы. Исследования показали, что
спинной мозг млекопитающих может являться самостоятельным, независимым от головного
мозга, генератором ритмичной локомоторной активности, обеспечивая выполнение
многих функций, необходимых для ходьбы [Rossignol S., Dubuc R., 1994]. Эта спинальная
активность контролируется и модулируется как супраспинальными нисходящими влияниями,
так и сенсорной афферентацией. Усиление потока сенсорных импульсов может улучшить
восстановление локомоторных функций после спинномозговой травмы за счет активизации
пластических возможностей сохранных отделов спинного мозга ниже уровня повреждения,
на этом основан метод сенсомоторной стимуляции. Этот метод предполагает активные
тренировки двигательных функций с использованием гравитационных нагрузок, тренировок
на тредбане; показана клиническая эффективность методик кинезотерапии, основанных
на применении метода сенсомоторной стимуляции [Chau С. и соавт., 1998]. Вызывать
или модулировать нужный спинальный локомоторный паттерн пытаются и с помощью
усиления супраспинальной афферентации, используя агонисты серотонина или норадреналина
- моноаминов, играющих важную роль в осуществлении контроля за сенсомо-торными
функциями. С этой же целью делаются попытки трансплантации эмбриональных моноаминергических
нейронов в спинной мозг ниже уровня травмы; результы, полученные в экспериментах
на животных, доказывают перспективность такого подхода [Feraboli-Lohngerr D.
и соавт., 1997].
Таким образом, значительный прогресс в отдельных областях нейробиологии, произошедший
в последнее десятилетие, открывает новые возможности для исследования процессов,
происходящих в травмированном спинном мозге, на клеточном и молекулярном уровнях.
Соответственно появляются надежды и на принципиально новые возможности реабилитации.
В настоящее время наиболее перспективным представляется комбинированное применение
трех вышеописанных стратегических подходов, позволяющее обеспечить оптимальную
базу для успешных вмешательств в процесс восстановления функций после спинно-мозговой
травмы [М.Ribotta, А.Privat., 1999].
9.3. РЕАБИЛИТАЦИЯ БОЛЬНЫХ С ПОЗВОНОЧНО-СПИННОМОЗГОВОЙ
ТРАВМОЙ В ПРОМЕЖУТОЧНОМ И ПОЗДНЕМ ПЕРИОДАХ
В промежуточный период, после полного исчезновения проявлений спинального
шока, формируется истинная картина двигательных расстройств. Усилия реабилитологов
направлены на восстановление двигательных функций (улучшение опорной функции
позвоночника и стимулирование еще продолжающихся в этот период восстановительных
процессов в спинном мозге, снижение повышенного мышечного тонуса при спастических
параличах либо стимуляция мышц при вялых параличах), на ликвидацию часто развивающегося
в этот период болевого синдрома, на предупреждение вегетативной дисрегуляции
и гетеротопической оссификации, на дальнейшее восстановление функции тазовых
органов, на социальную реадаптацию пострадавшего.
9.3.1. Восстановление двигательных функций
Для стимуляции восстановительных процессов в спинном мозге применяют
медикаментозные средства и физиотерапию, характер которых не отличается существенно
от используемых в раннем периоде.
В восстановлении функций позвоночника (в первую очередь - опорной) решающую
роль играет кинезотерапия. К основным задачам лечебной гимнастики в этот период
относятся: улучшение кровообращения в зоне поврежденного позвоночно-двигательного
сегмента, укрепление мышц спины и живота, плечевого и тазового пояса, формирование
мышечного корсета и правильной осанки, подготовка к дальнейшему расширению двигательного
режима. Вначале кинезотерапия проводится в палате, в формах индивидуальной активной
и пассивной гимнастики. Койки необходимо оборудовать балканскими рамами с передвигающимися
блоками, что позволяет проводить занятия в палате и существенно расширять комплекс
индивидуальной гимнастики.
В комплекс лечебной гимнастики включаются упражнения, в которых участвуют не
только конечности, но и сам позвоночник (таблица 9.6).
Таблица 9.6. ПРИМЕРНЫЙ КОМПЛЕКС ЛЕЧЕБНОЙ ГИМНАСТИКИ В ПРОМЕЖУТОЧНОМ
ПЕРИОДЕ ПОЗВОНОЧНО-СПИННОМОЗГОВОЙ ТРАВМЫ НИЖНЕГРУДНОГО, ПОЯСНИЧНОГО ОТДЕЛОВ
ПОЗВОНОЧНИКА
(по В.Н.Мошкову, 1984)
Лежа на спине
1. Руки вдоль туловища. Поднять руки вверх - вдох, опустить - выдох. 4-5 раз.
2. Свободно шевелить пальцами рук и ног.
3. Сгибание и разгибание стоп. 8-10 раз.
4. Круговые движения стопами. 8 раз в каждую сторону.
5. Ноги на ширине плеч. Повернуть стопы носками кнутри - кнаружи. 6-8 раз.
6. Поочередно приставить ноги к туловищу, согнув в коленях (на счет 1-2) -
выпрямить (на счет 3-4). 4-5 раз.
7. Смена положения рук: левая рука - вверх, правая - вниз. 10-12 раз.
8. Руки выпрямлены над головой. Тянуть руки вверх, пятки вперед, носочки на
себя (на счет 1-2-3-4) - расслабиться (на счет 5-6-7-8). 4-5 раз.
9. Поочередное отведение прямых ног в сторону (скользя пяткой по полу). 4-5
раз в каждую сторону.
10. Поочередное поднимание прямых ног вверх до угла 45°. 4-5 раз каждой ногой.
11. Приподнять ногу и. скрестив ее с другой (сгибая в колене), достать носочком
пол (не поворачивать корпус!), 4-5 раз каждой ногой.
12. Надавить носочками (от себя) на руки инструктора, напрягая мышцы ног (на
счет 1-2-3-4), расслабиться (на счет 5-6-7-8). 3-4 раза.
13. Поднять руки вверх - вдох, опустить - выдох. 3-4 раза.
14. Надавить носочками (на себя) на руки инструктора, напрягая мышцы ног (на
счет 1-2-3-4), расслабиться (на счет 5-6-7-8). 3-4 раза.
15. Левая нога приподнята, согнута в колене, правая выпрямлена на полу. "Велосипед"
левой ногой. 12-16 раз в каждую сторону. То же правой ногой.
16. Диафрагмальное дыхание. 7-8 раз.
17. Руки выпрямлены вдоль туловища. Приподнять таз, опираясь на лопатки и
стопы (на счет 1-2), расслабиться (на счет 3-4). 5-6 раз.
18. Ноги выпрямлены, между стопами медицинский мяч. Сжать мяч, напрягая мышцы
ног (на счет 1-2-3-4) - расслабиться (на счет 5-6-7-8). 4-5 раз.
19. Приставить левую ногу к туловищу, согнув ее в колене (на счет 1) - приподнять
пятку от пола с опорой на носок (2) - опустить пятку (3) - выпрямить ногу
(4). То же правой ногой. 3-4 раза каждой ногой.
20. Ноги выпрямлены, мяч между коленями. Сжать мяч, напрягая мышцы ног (на
счет 1-2-3-4) - расслабиться (на счет 5-6-7-8). 4-5 раз.
21. Диафрагмальное дыхание. 5-6 раз.
Лежа на животе
22. Попеременное сгибание и разгибание ног в коленных суставах. 16-20 раз.
23. Попеременное отведение прямых ног в стороны (скользя носочками по полу).
4-5 раз в каждую сторону.
24. Руки вверх. Прогнуться назад, приподняв верхнюю часть туловища (на счет
1-2-3), расслабиться (на счет 4-5-6-7-8-9-10). 6-8 раз.
25. Руки согнуты в локтях, ладони опираются на пол на уровне груди. Выпрямив
руки, приподнять верхнюю часть туловища от пола (на счет 1-2), вернуться в
исходное положение (на счет 3-4). 4-5 раз.
26. Руки вверх. Прямые руки и прямые ноги приподнять от пола (на счет 1-2-3),
расслабиться (на счет 4-5-6-7-8-9-10). 6-8 раз.
27. Попеременные движения прямыми руками вверх-вниз. 10-12 раз.
28. Руки согнуты в локтях, ладони на полу на уровне плеч. Свести лопатки,
напрягая мышцы спины (на счет 1-2-3-4) - расслабиться (на счет 5-6-7-8). 3-4
раза.
29. Выпрямить ноги, опираясь на носки и приподняв колени от пола; напрягать
мышцы ног, сжимать ягодицы (на счет 1-2-3-4-5) - расслабиться (на счет 6-7-8-9-10).
3-4 раза.
30. Прямые руки в стороны. Приподнять руки от пола, удержать в таком положении
(на счет 1-2-3-4), опустить (на счет 5-6-7-8). 5-6 раз.
31. Повторить предыдущее упражнение с дополнительным отягощением (взяв в руки
гантели; надавливая на руки инструктора). 3-4 раза.
32. Прямые руки в стороны, кисти сжаты в кулачки. Приподнять руки от пола,
выполнять круговые движения прямыми руками, напрягая мышцы. 8-10 раз в каждую
сторону.
Стоя на четвереньках
33. Поочередное отведение прямых рук в стороны. 8-10 раз.
34. Поочередные маховые движения прямыми ногами назад. 8-10 раз.
35. Выпрямить правую ногу назад, скользя носочком по полу, садясь при этом
на левую пятку (на счет 1-2) - вернуться в исходное положение (3-4). То же
другой ногой. 4-5 раз каждой ногой.
36. Выполнить маховое движение прямой ногой назад с одновременным поднятием
разноименной руки вверх, удержать (на счет 1-2-3-4) - вернуться в исходное
положение (на счет 5-6-7-8). 3-4 раза каждой ногой и рукой.
37. Сесть на пятки, не отрывая рук от пола (на счет 1-2) - вернуться в и.п.
(3- 4). 5-6 раз.
38. Упражнение "кошечка" (прогибать спину дугой вниз). 7-8 раз.
Лежа на спине
39. Ноги выпрямлены, руки вдоль туловища. Диафрагмальное дыхание.
40. Руки вверх, пятки тянуть вперед, носки на себя - вдох, руки опустить,
расслабиться - выдох. 4-5 раз.
41. Попеременное тыльное и подошвенное сгибание стоп. 10-12 раз.
42. Руки вверх - вдох, опустить - выдох. 3-4 раза.
43. Свободное дыхание. 30-40 сек.
По мере формирования мышечного корсета и при условии стабильности позвоночно-двигательных
сегментов добавляются следующие формы кинезотерапии: вертикальная установка
больного, занятия в группе, упражнения с самовспоможением, локомоторные упражнения,
упражнения по развитию навыков самообслуживания. Для уменьшения ортостатических
реакций периодически (3-4 раза в день) больному рекомендуют спускать поочередно
ноги с кровати вниз вначале на 5-10 минут, а затем постепенно увеличивая время
до 30 минут. Необходимо также поднимать головной конец кровати для придания
больному полусидячего положения.
Для перемещения больного в вертикальное положение используют поворотный стол
или специальную поворотную кровать. При помощи механической передачи регулируют
уровень наклона стола, постепенно переводя его в вертикальное положение. Примерная
схема проведения процедур приведена в таблице 9.7.
Таблица 9.7. ПРИМЕРНАЯ СХЕМА ПЕРЕВОДА БОЛЬНОГО В ВЕРТИКАЛЬНОЕ ПОЛОЖЕНИЕ
(по Т.Н.Кукушкиной и совет., 1981)
Порядковый номер занятия |
Величина угла в градусах |
Время занятия в минутах |
| первое занятие |
45
65
85
65
45 |
10
5
5
5
5 |
| второе занятие |
45
65
85
65
85
65
45 |
10
5
5
5
5
5
5 |
Третье занятие проводят аналогично второму, выполняя из положения под углом
45 градусов пассивные движения в суставах верхних конечностей в медленном
темпе, сочетая их с глубоким дыханием. На следующем занятии больного троекратно
поднимают до угла в 85 градусов, длительность занятия достигает 50 минут.
В дальнейшем пассивные движения в суставах конечностей производят из положений
с более высоким углом подъема больного, увеличивая продолжительность занятия
до 1 часа. Около больного постоянно должен находиться методист, контролирующий
состояние больного во время процедуры. Иногда (по показаниям) перед процедурой
целесообразно введение кордиамина.
Пациент, фиксированный ремнями к поворотному столу, может выполнять упражнения
для укрепления мышц верхних конечностей. При отстегивании ремня, фиксирующего
грудную клетку, начинают применять упражнения на равновесие, наклоны туловища
в различных плоскостях. Вначале упражнения выполняют при помощи методиста,
затем с опорой на барьер, на поручни поворотного стола.
После вертикальной установки больного (которую можно считать завершенной
при пребывании больного в положении стоя в течение 1 часа) начинается самостоятельное
усаживание больного. Больных с повреждением спинного мозга на уровне шейного
и верхнегрудного отдела усаживают и поддерживают в положении сидя в инвалидном
кресле-каталке. Одновременно с вертикальной установкой больного применяют
упражнения для укрепления мышц туловища, обучают навыкам перехода в следующие
позиции: лежа на животе, на боку, сидя на коленях и пятках, на четвереньках;
обучают переходу из положения на четвереньках в положение сидя на правой и
левой ягодицах с возвратом в положение на четвереньках, из положения лежа
на животе в положение сидя с выпрямленными ногами, из положения лежа на животе
в положение сидя на правой или левой ягодице, из положения сидя с выпрямленными
ногами в положения лежа на животе.
Обучение стоянию проводится с помощью коленодержателей и манежей.
Необходимо подчеркнуть важность ежедневного пребывания пациента в положении
"стоя". Вертикальная поза обеспечивает нагрузку нижних конечностей,
способствуя предотвращению развития остеопороза и контрактур, стимулирует
кровообращение, способствует улучшению функции почек [Jaeger R. еt а1, 1990].
С целью восстановления устойчивости вертикальной позы проводят также электростимуляцию
широких мышц спины, косых и прямых мышц живота. Время стояния увеличивают
постепенно и доводят до 2-3 часов.
Затем приступают к обучению ходьбе. При обучении ходьбе руководствуются
уровнем и видом повреждения спинного мозга. При повреждении шейного или верхнегрудного
отдела (выше уровня Тh6 сегмента) единственным способом передвижения является
инвалидное кресло-каталка. При частичной травме спинного мозга выше Тh6 сегмента
или полном поражении на более низком уровне обучают самостоятельному передвижению.
При клинике полного повреждения спинного мозга обучают ходьбе при стабилизации
ног в ортопедических аппаратах. Начинают ходьбу в барьерах (брусьях) или ходунках.
Вначале осваивают положение стоя (необходимо контролировать положение головы
и туловища, следить за правильным дыханием). Затем больному предлагают самому
следить за осанкой, выполнять дыхательные упражнения, переносить тяжесть тела
с одной ноги на другую; затем с помощью методиста пытаться делать шаги вперед,
назад, вправо, влево. После каждого задания - отдых в течение 1-2 мин с выполнением
дыхательных упражнений.
Для обучения ходьбе очень эффективно использование подвесной монорельсовой
"дороги", которую можно соорудить в гимнастическом зале, в коридоре,
в бассейне. На больного надевают специальный жилет с фиксирующими устройствами
и "подвешивают" к монорельсе, уменьшая таким образом воздействие
силы тяжести тела и облегчая перемещение. Занятия проводят через день. Продолжительность
занятия вначале составляет 15-20 минут, затем постепенно увеличивается до
1 часа (усложняются задачи, увеличивается количество шагов, уменьшается помощь
методиста.
В настоящее время разрабатываются системы функциональной нервномышечной стимуляции,
предназначенные для стимуляции мышц ног и тазового пояса во время стояния
и ходьбы [Yarkony G. и соавт., 1992]. Элементы электростимуляции используют
также в комбинации с ортезами, однако стоимость таких ортезных систем очень
велика.
После освоения ходьбы в ходунках либо по монорельсовой "дороге"
приступают к обучению ходьбе на костылях (необходимо научить больного правильно
падать: при потере равновесия костыли разводят в стороны либо бросают и стараются
упасть на полусогнутые руки, напрягая мышцы). По мере овладения навыками ходьбы
переходят на ходьбу с двумя тростями, затем с одной и, наконец, без трости.
После освоения ходьбы по горизонтальной поверхности приступают к ходьбе по
наклонной плоскости, лестнице, продолжают тренировать падать и вставать (навыки
безопасного падения на руки и вставания уменьшают опасения больного перед
падением, способствуют самостоятельному хождению без страховки). Активность
и эффективность ходьбы зависит от уровня повреждения спинного мозга. Как правило,
без ограничений могут овладеть навыками ходьбы пациенты с повреждением спинного
мозга ниже уровня L2 сегмента.
Лечебные мероприятия при спастических и вялых параличах
Спастичность в парализованных мышцах (при поражении верхнего мотонейрона)
обычно развивается постепенно, в течение первых 3-х месяцев после травмы.
Вначале мышечный тонус преобладает в мышцах-сгибателях конечностей, однако
со временем спастичность начинает доминировать в разгибателях [Merrit J.,
1981]. Лечебные мероприятия, направленные на снижение мышечного тонуса, назначают
в тех случаях, когда спастичность приводит к нарушению самообслуживания, походки,
вызывает боль, дискомфорт или нарушение сна, способствует развитию пролежней
и контрактур. Однако иногда повышенный тонус мышц-разгибателей бедра и голени
способствует удержанию вертикальной позы, стоянию и передвижению, и в таких
случаях резко снижать его нецелесообразно.
Мероприятия по уменьшению мышечого тонуса заключаются в предотвращений резких
болевых и проприоцептивных раздражений конечностей, которые способствуют увеличению
спастичности, в выполнении постоянных упражнений на растяжение мышц, приеме
миорелаксантов, в выполнении спирт-новокаиновых, феноловых блокад или местном
введении ботулотоксина. Все эти мероприятия подробно описаны в главе
4.1. Отметим лишь, что среди лекарственных средств-миорелаксантов
препаратом выбора для больных с повреждением спинного мозга является баклфен.
При вялых параличах назначаются ноотропные средства, стимулирующие
мышцы физиотерапевтические процедуры, особое внимание уделяется электростимуляции
мышц. При поражении на уровне С5-С8 сегментов спинного мозга вялый паралич
развивается в мышцах верхних конечностей, при поражении на уровне L1-S1 -
в мышцах нижних конечностей. Принципы и методика стимуляции паретичных мышц,
а также особенности массажа, лечебной гимнастики и рефлексотерапии при вялых
параличах изложены в главе 4.2.
С помощью многоканальной электростимуляции (на аппарате типа "Миотон")
осуществляется тренировка шаговых движений для нижних конечностей и хватательных
для верхних. Процедуры электростимуляции использует также для укрепления мышц
спины и живота (обеспечение устойчивости вертикальной позы).
В позднем периоде (не ранее чем через 1 год после травмы) при стабильно необратимых
двигательных нарушениях (отсутствие положительной динамики на протяжении 6
месяцев) иногда прибегают к ортопедическим вмешательствам, направленным на
улучшение функции конечности и повышение степени самообслуживания. Важным
условием таких вмешательств является наличие у больного мотивации к активному
использованию конечности и его информированность относительно целей и ожидаемых
результатов операции. Возможным ограничением к выполнению ортопедического
пособия может стать значительное повышение мышечного тонуса. Существует значительное
число оперативных техник по восстановлению активного сгибания руки в локтевом
суставе, разгибанию кисти, формированию щипкового охвата и других функций
верхней конечности. Наиболее распространены операции перемещения мышечных
сухожилий. Так, активное разгибание руки в локтевом суставе может быть достигнуто
соединением задней порции дельтовидной мышцы с сухожилием трехглавой мышцы
плеча при помощи свободных сухожильных вставок. Восстановление разгибания
в кистевом суставе может быть достигнуто перемещением сухожилия плечелучевой
мышцы к месту прикрепления короткого лучевого разгибателя кисти. При выполнении
операций по перемещению сухожилий руководствуются следующими условиями [Johnstone
и соавт., 1988]:
- перемещаемая мышца должна иметь достаточную для выполнения планируемой функции
силу;
- перемещаемая мышца должна быть синергистом по отношению к восстанавливаемому
движению;
- сустав, функцию которого восстанавливают, должен иметь полный объем пассивных
движений;
- в первую очередь восстанавливают функцию доминантной руки (если только двигательные
и чувствительные функции на недоминантной стороне не являются значительно
более сохранными).
После оперативного вмешательства в течение трех недель (при операциях на
кисти) или шести недель (при операциях на локтевом суставе) конечность иммобилизируют
в положении, не допускающем растяжения пересаженных мышц. Мобилизацию производят
очень постепенно и бережно, одновременно обучая пациента использованию новых
функциональных возможностей.
Продолжается лечение пролежней. При длительно незаживающих пролежнях
и трофических язвах прибегают к хирургическому лечению: используют методы
свободной кожной аутопластики (при поверхностных пролежнях в воспалительно-регенеративной
и регенеративной стадиях; при глубоких пролежнях у ослабленных больных, когда
неприемлемы более сложные пластические операции) либо местнопластические операции
с перемещением тканей.
9.3.2. Лечение нарушений функций тазовых органов (совместно с А.Г.Поляковой)
Лечение этих нарушений в промежуточном периоде ПСМТ направлено на выработку
пузырного рефлекса при гипотоническом пузыре и на выработку контролируемого
мочеиспускания при гипертонической форме нейрогенных расстройств. Направленность
мероприятий зависит от формы нейрогенной дисфункции, от соотношения тонуса
сфинктера и детрузора.
При формировании гиперрефлекторного мочевого пузыря выполняются
мероприятия, направленные на снижение его тонуса. Ниже приведены рекомендуемые
процедуры.
- ДМВ-терапия - слаботепловая доза, мощность 20-30 Вт, 8-10 мин; индуктор
располагается в надлобковой области без воздушного зазора, 6-8 процедур.
- Парафиновые или озокеритовые аппликации на область мочевого пузыря, температура
40-42°, 20-25 мин, 8-10 процедур.
- Электрофорез М-холинолитиков, спазмолитиков (атропин 1%, галантамин, ганглерон,
но-шпа, платифиллин, папаверин) и миорелаксантов (фенибут и др.), поперечное
расположение электродов (один - над лонным сочленением, другой - в области
крестца); плотность тока 0,03-0,05 мА/см кв., время - 12 мин, 10-15 процедур.
- Сегментарный массаж, точечный массаж надлобковой области.
- Вибромассаж сегментарной и надлобковой области - частотой 50- 100 Гц, по
10 мин, курсом 15-20 процедур, при отсутствии клинического улучшения - повторение.
- Пресакральные новокаиновые блокады в сочетании с блокадой срамных нервов:
применяются для воздействия на периферическое звено рефлекса мочеиспускания
и создания координированных взаимоотношений в системе "детрузор-сфинктер".
Согласно методике С.Д. Серегиной, в случае повышенного сопротивления наружного
сфинктера в крестцовый канал вводят по 0.1 мл официнальных растворов прозерина
и стрихнина на 4-5 мл физиологического раствора, эту процедуру повторяют второй
раз через день. При отсутствии патологической реакции на эндосакральное введение
данных препаратов в последующем в крестцовый канал вводят по 1 мл стрихнина
и прозерина на 4-5 мл физиологического раствора через день, 7-10 блокад. Для
создания координированных взаимоотношений в работе детрузора и сфинктера мочевого
пузыря одновременно проводят блокады срамных нервов.
- ИРТ (тормозной метод): постепенно нарастающая интенсивность раздражения,
длительность нахождения иглы в тканях от 25 до 50 минут. С целью уменьшения
расстройств функций тазовых органов используют точки как общего, так и локально-сегментарного
действия. При задержках мочеиспускания применяют иглорефлексотерапию слабым
тормозным методом в точки цюй-гу XIV (J)-2, чжун-цзи XIV (J)-3, гуань-юань
XIV (J)-4, ши-мэнь XIV (J)-5, сан-инь-цзяо IV (RР)-6, шан-цю IV (RР)-5, шэнь-шу
VII (V)-23, ци-хай-шу VII (V)-24, да-чан-шу VII (V)-25, гуань-юань-шу VII
(V)-26. При этом целесообразно в первый день использовать точки нижней части
живота и внутренней поверхности ног, на второй день - сегментарные точки пояснично-крестцовой
области. По методике А.С. Цогоева и А.Т. Качана [1996] наиболее эффективным
является сочетание точек, располагающихся над верхним краем лонной кости:
цюй-гу XIV (J)-2, хэн-гу VIII (R)-11. На ногах предпочтение отдается точкам
канала селезенки - поджелудочной железы: IV (RР)-6 сан-инь-цзяо, IV (RР)-9
инь-линь-цю-ань и IV (RР)-10 сюе-хай. При введении иглы желательно добиваться
предусмотренных ощущений в виде иррадиации в область промежности. Экспозиция
игл в тканях составляет 30-40 минут с постоянным их вращением. Если удается
добиться самостоятельного мочеиспускания, то в дальнейшем экспозицию уменьшают
до 25 минут за сеанс. Курс лечения 10-12 процедур, проводят с перерывами 3-4
курса.
- Наружная электростимуляция мочевого пузыря: применяется для преимущественного
воздействия на детрузор мочевого пузыря, осуществляется при гиперрефлекторном
мочевом пузыре по тормозной методике, диадинамическими или синусоидальными
модулированными токами. Два электрода размерами 10 х 10 см накладывают над
лобком по бокам от средней линии живота (воздействие осуществляется преимущественно
на детрузор).
Стимуляция диадинамическими токами: последовательно включают двухтактный
ток на 2 минуты, короткий период на 3 минуты, длинный период на 2 минуты.
Сила тока от 5 до 20 мА, курс 6-12 процедур. Проводят 2-3 курса с перерывами
между курсами в 10-15 дней.
Стимуляция синусоидальными модулированными токами [Ясногородский В.Г.,
1985]: применяют немодулированные колебания (I род работ, глубина модуляции
0%), 7-14 мА, в течение 10 минут, ежедневно, 10- 12 процедур.
- Трансректальная электростимуляция: применяется для преимущественного воздействия
на сфинктер мочевого пузыря. При тормозной методике катод располагают над
лоном, анод - ректально. При стимуляции синусоидальными модулированными токами
используют выпрямленный режим, III-IV род работ, глубину модуляции 50-75%,
частоту 150-100 Гц, длительность посылок тока по 3 сек., 5-6 минут на процедуру,
курс - 10-12 процедур. Трансректальная электростимуляция противопоказана при
желудочно-кишечных кровотечениях, некротических дистрофических процессах в
желудочно-кишечном тракте, сердечно-сосудистой недостаточности.
Необходимо помнить, что детрузорно-сфинктерная диссинергия и высокое давление
в мочевом пузыре может привести к рефлюксу мочи и развитию гидронефроза. Поэтому
необходимо динамическое урологическое обследование больных.
При формировании гипорефлекторного мочевого пузыря назначают
процедуры, направленные на повышение его тонуса.
- Электрофорез прозерина, пилокарпина на область мочевого пузыря, поперечное
расположение электродов; плотность тока 0,03-0,05 мА/см кв., время - 12 мин,
№ 10-15.
- Грязевые аппликации соответственно очагу поражения спинного мозга, температура
аппликаций 42-44°, время аппликации 20 мин, курс 12- 15 процедур.
- ИРТ по возбуждающей методике: сильное короткое раздражение с длительностью
оставления иглы в тканях от 10 минут при первых процедурах с постепенным уменьшением
до 5-3 минут при последующих. При недержании мочи основными точками являются
ней-гуань IX (МС)-6 и чжао-хай VIII (R)-6. Кроме того, рекомендуются шан-ляо
VII (V)-31, вей-чжун VII (V)-40, шэнь-май VII (V)-62, сан-инь-цзяо IV (RР)-6,
инь-лин-цуань IV (RР)-9, бай-хуэй XIV (Т)-20, пан-гуань-шу VII (V)-28. На
все точки производится тонизирующее воздействие. При ослаблении сфинктера
мочевого пузыря - цзу-сань-ли III (Е)-36. Добавочные точки да-чан-шу VII (V)-25,
сяо-чан-шу VII (V)-27, пан-гуан-шу VII (V)-28.
По методике предложенной А.С. Цогоевым и А.Т. Качаном [1996], экспозиция игл
в тканях при первой процедуре ИРТ при гипотонических синдромах составляет
от 1 минуты до 5 минут (проводят дифференцировано в зависимости от состояния
тонуса детрузора и сфинктера мочевого пузыря). Рецептура составляется из точек
канала селезенки - поджелудочной железы (аналогично рецепту при гипертоническом
синдроме). Если наблюдается улучшение (клинически или по результатам цистометрии),
проводят еще 3 сеанса с более короткой или более длительной экспозицией. При
подборе рецепта необходимо помнить, что различные варианты сочетания точек
дают эффект суммации без адаптации только после 3-4-х процедур. Последующие
сеансы требуют смены рецептуры и перехода к использованию точек каналов почек
и печени: шуй-цюань VIII (R)-5, чжао-хай VIII (R)-6, да-чжун VIII (R)-4; чжун-фэн
XII (Р)-4, ли-гоу XII (Р)-5, цзу-у-ли XII (Р)-10 и т.д.). Точки, расположенные
на наружных ножных каналах в рецептуру не включаются из-за противоположного
влияния их на двигательную функцию конечностей. Поэтому предпочтение отдается
стимуляции точек каналов мочевого пузыря и заднего срединного на уровне и
выше уровня травмы. Воздействие на них параллельно улучшает крово- и лимфоток,
способствует быстрейшему снятию отека и ускоряет процесс регенерации. Если
удается добиться эффекта, то переходят на гармонизирующий метод с экспозицией
игл в точках акупунктуры - 15 минут. Необходимо следить за тем, чтобы во время
сеанса ИРТ мочевой пузырь не был пустым или переполненным. Между сеансами
ИРТ и физиотерапии выдерживается перерыв не менее 2-х часов.
При сопутствующей импотенции в рецептуру включаются точки ян-гу VI (YG)-5,
сан-инь-цзяо IV (RР)-6, ци-хай XIV (J)-6, хэн-гу VIII (R)-11, ци-чун III (Е)-36
[Вогралик В.Г., 1961; Чжу Лянь, 1959].
- Наружная электростимуляция мочевого пузыря диадинамическими или синусоидальными
модулированными токами (стимулирующая методика). Два электрода размерами 10х10
см накладывают над лобком по бокам от средней линии живота, либо используют
абдоминально-сакральное расположение электродов.
Стимуляция диадинамическими токами: последовательно включают двухтактный
ток 30 сек., однотактный ток и короткие периоды по 3 минуты, ритм синкопа
- 6 минут. Сила тока от 5 до 20 мА, курс 6-12 процедур. Проводят 2-3 курса
с перерывами между курсами в 10-15 дней [Сосин И.Н. и соавт., 1996].
Стимуляция синусоидальными модулированными токами [Ясногородский В.Г.,
1985]: II род работ, частота модуляции 20-30 Гц, длительности посылок тока
и пауз по 5 сек.; силу тока повышают до сокращения мышц брюшной стенки (15-45
мА), продолжительность процедуры 10 минут, ежедневно, 10-12 процедур на курс.
- Трансректальная электростимуляция: расположение электродов - анод над лонным
сочленение, катод - ректально. При стимуляции синусоидальными модулированными
токами используют выпрямленный режим, II род работ с частотой импульсов 20-30
Гц, глубиной модуляции 100%, длительностью полупериодов по 2-3 сек., сила
тока - до выраженной вибрации, продолжительность процедуры 5-6 минут на процедуру,
курс - 10-15 процедур [Антропова М.И., 1983].
Выработку пузырного рефлекса осуществляют путем регулярных тренировок мочевого
пузыря. Такая тренировка заключается в том, что больному предлагается вначале
каждые 1-2 часа, затем через более длительные промежутки времени пытаться самостоятельно
помочиться, помогая себе натуживанием и надавливанием руками на переднюю брюшную
стенку. Для выработки пузырного рефлекса можно использовать также систему Монро:
с помощью правильно подобранной высоты колена отводящей трубки приучают детрузор
к сокращению в нормальном режиме.
Если с помощью системы Монро пузырный рефлекс удается выработать лишь через
6-12 месяцев, то с помощью трансректальной электростимуляции, по данным А.В.Лившица
[1994] - в сроки до 1 месяца. Однако могут наблюдаться случаи, когда электростимуляция
в большей степени усиливает сократительную способность сфинктера и в меньшей
- детрузора (объем остаточной мочи после одного или двух 10-14-суточных курсов
трансректальной стимуляции более 100 мл). В этих случаях при сохранении возбудимости
детрузора некоторые отечественные авторы рекомендуют непосредственную электростимуляцию
мочевого пузыря путем имплантации оперативным путем радиочастотного стимулирующего
устройства (эти операции производятся уже в промежуточном периоде ПСМТ). Методика
радиочастотной стимуляции мочевого пузыря при помощи имплантируемых электродов
детально разработана А.А. Вишневским и А.В. Лившицом [1973] и описана в монографии
этих авторов (Вишневский А.А., Лившиц А.В. Электростимуляция мочевого пузыря.-
М.: Медицина, 1973.).
В случаях, когда произвольное мочеиспускание не восстанавливается, продолжают
проводить периодическую катетеризацию, а между сеансами катетеризации применяют
антихолинэстеразные средства либо спазмолитики.
При наличии надлобкового свища в позднем периоде травмы необходимо добиться
выработки произвольного или автоматического акта мочеиспускания и ликвидации
цистостомы. Показаниями к закрытию цистостомы является наличие пузырного рефлекса
и возможность мочеиспускания по уретре, т.е. ее проходимость. Наличие пузырного
рефлекса проверяется с помощью цистометрии. При подготовке к закрытию цистостомы
большое значение имеет тренировка мочевого пузыря с целью увеличения его емкости,
выработки пузырного рефлекса. Для этого вначале к дренажной трубке подключают
систему Монро. Постепенно отводящий конец тройника поднимают на 20-30-40 см
над уровнем лобка. Дозированное повышение давления в мочевом пузыре способствует
увеличению объема сморщенного пузыря (который всегда является результатом эпицистостомии),
выработке пузырного рефлекса для нормального акта опорожнения. Наличие антисептической
жидкости, подбираемой в зависимости от чувствительности микрофлоры мочи, позволяет
проводить тренировку пузырного рефлекса без опасения обострения инфекции. По
мере выработки пузырного рефлекса и восстановления нормального или автоматического
мочеиспускания через уретру при достаточном объеме мочевого пузыря, отсутствии
обострения воспалительного процесса и большого количества остаточной мочи дренажную
трубку перекрывают на несколько дней, а затем убирают. Катетеризируют мочевой
пузырь постоянным катетером на 7-9 дней, для того, чтобы закрылось отверстие
на передней брюшной стенке. После этого больной самостоятельно опорожняет мочевой
пузырь.
При сформировавшемся вторично сморщенном мочевом пузыре (органический арефлекторный
мочевой пузырь объемом 10-15 мл) в позднем периоде ПСМТ возникают показания
для илеоцистопластики. Повздошно-кишечная пластика арефлекторного органического
мочевого пузыря обеспечивает естественное управляемое мочеиспускание и позволяет
в определенной степени защитить почки от восходящей инфекции. Тем не менее опасность
такого инфицирования весьма велика.
Оценку эффективности коррекции тазовых нарушений производят с учетом достигнутой
степени компенсации. Различают 4 степени компенсации тазовых функций [Перльмуттер
О.А., 2000].
При оптимальной степени компенсации мочеиспускания больной может
удерживать мочу в течение 4-5 часов при емкости пузыря 250-350 мл. Остаточной
мочи нет. Больные чувствуют наполнение пузыря или его косвенные признаки в виде
своеобразных ощущений - тяжесть внизу живота, покалывание, жжение в области
мочевого пузыря, у них может возникать гиперемия лица, резкая потливость, после
чего происходит акт мочеиспускания.
Удовлетворительная степень компенсации предполагает удерживание
мочи 2-2,5 часа и осуществление мочеиспускания произвольно или с натуживанием.
Емкость мочевого пузыря 200-250 мл, остаточной мочи 50-70 мл. Позыв и ощущение
прохождения мочи по уретре слабо выражены.
Минимальная степень компенсации устанавливается у лиц с недостаточным
контролем мочеиспускания. Мочевой пузырь опорожняется часто (через 30-60 мин),
нередко при интенсивном натуживании, выделяется малое количество мочи (40-70
мл). Отсутствует позыв, чувство наполнения и прохождения мочи по уретре. Нередко
мочеиспускание непроизвольное или императивное. При физическом напряжении, перемене
положения тела моча не удерживается. Емкость мочевого пузыря, как и количество
остаточной мочи зависят от тонуса детрузора и сфинктера (при гипотонии детрузора
в пределах 500- 700 мл, при гипертонии - 20-125 мл).
Неудовлетворительной степенью компенсации считается состояние
больных, при котором акт мочеиспускания полностью не контролируется, непроизвольное
мочеиспускание происходит либо каждые 10-30 мин, либо наблюдается полное недержание
мочи, либо ее полная задержка. Отсутствуют чувство наполнения, позыв и прохождение
мочи и катетера по уретре. Емкость пузыря при гипотонии детрузора 500-800 мл,
остаточной мочи - 500-700 мл, при гипертонии детрузора емкость 20-50мл.
Мероприятия, назначаемые для установления контролируемого акта дефекации, также
зависят от характера нейрогенных расстройств [Коган О. Г., Найдин В.П., 1988].
При гипотоническом запоре назначают процедуры, усиливающие перистальтику
кишечника.
- Питуитрин и прозерин подкожно.
- Пероральный прием слабительных, свечи с бисекодилом.
- Электрофорез прозерина на область кишечника.
- Наружная электростимуляция кишечника синусоидальными модулированными токами
или диадинамическими токами: один электрод располагают сегментарно (пояснично-крестцовая
область), второй - на брюшной стенке (в области проекции сигмовидной или слепой
кишки) [Ясногородский В.Г., 1985].
Стимуляция синусоидальными модулированными токами: используют II род
работ, частоту модуляции 30 Гц, глубина модуляции 75-100%, длительность посылок
и пауз по 5 сек., сила тока 25-30 мА, 10-20 процедур.
Стимуляция диадинамическими токами: используют однополупериодный волновой
ток, интенсивность тока, вызывающую ощущение выраженной, но безболезненной
вибрации под электродами, длительность процедуры - 20-30 минут, 10-20 процедур
на курс.
Возможна также электроимпульсная стимуляция кишечника ректальным электродом.
- Гидромассаж живота и сегментарной зоны, струевой, 1.5 атм, 10 мин, №10.
- Сегментарный массаж, массаж живота с использованием элементов точечного,
тонизирующим методом.
- ИРТ по возбуждающей методике: при атонии кишечника - ци-хай XIV (J)-6,
шень-цюе XIV (J)-8, основная точка - ней-гуань IX (МС)-6, а также цзу-сань-ли
III (Е)-36, да-чан-шу VII (V)-25, нао-шу VI (YG)-10 (рекомендуется прижигание).
При паралитическом илеусе добавляются точки тянь-шу III (Е)-25, вай-лин III
(Е)-26 и тай-чун XII (Р)-3.
- Грязевые прямокишечные тампоны.
- Лечебная гимнастика для мышц живота и тазового пояса.
Очень важна диета, включающая растительную клетчатку и не допускающая ограничения
жидкости.
При синдроме спастического запора назначают процедуры, направленные
на нормализацию тонуса мускулатуры кишечника.
- Электрофорез спазмолитиков (платифиллина, но-шпы, атропина) на область кишечника,
располагая электроды продольно по ходу кишечника слева и справа; сила тока
до минимальных ощущений, время процедуры 12-15 мин, № 7-15.
- Ток Д'Арсонваля среднеискровым разрядом на сегментарную зону Тh6-L1 и область
живота по часовой стрелке (чередовать с электрофорезом), № 7-15.
- Наружная электростимуляция кишечника интерференционными токами с частотами
90-100Гц, располагая электроды поперечно на область живота, длительность процедуры
15 мин., № 6-12.
- Магнитотерапия на область живота, индукторы располагают по ходу спазмированных
отделов кишечника, импульсный режим, время воздействия 20-25 мин., № 15-20.
- Массаж живота и сегментарный массаж, курсом до 15 процедур.
- Грязевые и парафиновые аппликации на область живота, температура аппликаций
38-42°, 20-25 мин., № 10-12.
- Грязевые прямокишечные тампоны.
- ИРТ по тормозной методике. При спастических запорах основной точкой считается
гун-сунь IV (RР)-4, а также инь-лин-цуань IV (RР)-9, да-дунь XII (Р)-1, хуан-шу
VШ (R)-16.
- Электросон частотой 10-20 Гц, длительность импульсов 0,9-0,5 мcек, по глазнично-затылочной
методике, продолжительность сеанса 30 мин., № 6-10.
- Хвойные ванны, жемчужные ванны, температура воды 35-36°, 10 мин., № 10
через день.
В течение трех недель ежедневно производится очистка кишечника: энтеродез
и другие сорбенты через день чередуют с клизмами, отмывая кишечник до чистой
воды, чтобы избежать всасывания токсических продуктов. У некоторых больных
возможно применение трав со слабительным действием (ромашка, сенна), теплой
минеральной воды.
При недержании кала назначают процедуры стимулирующего действия.
- Инъекции прозерина, витаминов группы В, АТФ.
- ИРТ по возбуждающей методике.
- Электроимпульсная стимуляция кишечника ректальным электродом.
- Электрофорез грязи поперечно с расположением катода в надлобковой области,
анода в крестцовой области, плотность тока 0,03-0,04 мА/см кв., время воздействия
12- 15 мин., № 10-12.
- Лазеротерапия области промежности сканер-лазером и сегментарной пояснично-крестцовой
зоны, 6-8 минут на поле, курсом 12-15 процедур, с частотой 20 Гц или воздействия
приемами лазеропунктуры.
- Гидромассаж струевой на область живота, сегментарной зоны, области промежности,
передней поверхности бедер, 1.5 атм, 10 мин., № 10.
- Лечебная гимнастика для укрепления мышц тазового дна и брюшного пресса.
Лечение гипоэрекционного либо анэрекционного синдрома
включает назначение инъекций прозерина, витаминов, тонизирующих препаратов,
электрофорез прозерина на область промежности, сегментарный массаж, иглорефлексотерапию
по возбуждающему методу, ректальные грязевые тампоны [Коган О. Г., Найдин В.Л.,
1988]. Важная роль принадлежит психотерапевтической работе с обоими супругами.
Жену и мужа одновременно обучают новым сексуальным играм с использованием эректоров,
стимуляторов, с воздействием на эрогенные точки.
В промежуточном периоде начинаются, а в позднем - становятся основными реабилитационные
мероприятия, направленные на восстановление самообслуживания и, по возможности,
трудоспособности больного.
9.3.3. Социальная реадаптация и медико-социальная экспертиза пострадавших
9.3.3.1. Прогноз восстановления самообслуживания и трудоспособности
Способность больного к самообслуживанию и локомоции зависит от уровня повреждения
спинного мозга. При повреждении на уровне С6 сегмента возможна самостоятельная
езда в инвалидном кресле, на уровне С7 - самостоятельное одевание, еда, частичное
самообслуживание в быту, ограниченная способность к самостоятельному перемещению
из инвалидного кресла в постель и обратно, самостоятельная езда в инвалидном
кресле. При травме на уровне Тh1 сегмента - возможны самостоятельное одевание,
еда, самообслуживание в быту, ограниченное самостоятельное передвижение из инвалидного
кресла в ванную и обратно, самостоятельная езда в инвалидном кресле; на уровне
Тh6 сегмента - возможны самостоятельное одевание, еда, самообслуживание в быту,
самостоятельное перемещение из инвалидного кресла в постель и обратно, из инвалидного
кресла в ванную и обратно, из инвалидного кресла на пол и обратно, самостоятельная
езда в инвалидном кресле, не исключена ходьба с подмышечными костылями в высоких
аппаратах с поясом. При страдании на уровне L2 сегмента помимо перечисленных
навыков возможна ходьба с локтевыми костылями в высоких аппаратах, а с уровня
L5 - с локтевыми костылями в аппаратах до колен [Вейсс М., Зембатый А., 1986].
Трудотерапия и профессиональная ориентация решают задачу реинтеграции
пострадавшего в общество. Усилия реабилитологов направлены на возвращение больного
к учебе, привычной работе либо на обучение новой посильной профессии. К сфере
медицинской реабилитации относятся консультирование больного по поводу возможности
выполнять те или иные работы, тогда как профессиональная ориентация, переобучение
и трудоустройство становятся функцией служб социального обеспечения и социальной
защиты. К факторам, связанным с большей вероятностью возвращения больного к
труду, относятся [Stover S., Fine Р., 1986]: женский пол, высшее образование,
более каудальный уровень травмы спинного мозга, наличие мужа (жены), возраст
25-44 г, способность контролировать функции тазовых органов, материальный стимул.
Противопоказанные виды и условия труда [Амелина О.А., 1998]:
- связанные со статической нагрузкой, резкими и постоянными движениями в позвоночнике
и конечностях, с вынужденным положением туловища;
- связанные с воздействием неблагоприятных метеорологических факторов (особенно
охлаждение), токсических веществ;
- при параличах и парезах - связанные с физическим напряжением соответствующих
сегментов конечностей;
- при нарушениях тазовых функций - требующие постоянного нахождения на рабочем
месте (оператор, сборщик на конвейере и т.д.).
Одной из сфер деятельности, которая значительно расширяет социальные возможности
больного и может даже стать профессией, является вождение автомобиля. Обучение
больных автомобилевождению в условиях параличей нижних, а иногда и верхних конечностей,
требует участия врача-консультанта (оценка функциональных возможностей пациента),
инженера (осуществляет необходимое техническое переоборудование автомобиля),
инструктора по вождению. В некоторых странах (например, в США) существуют специальные
программы для больных ПСМТ по обучению вождению, эти программы поддерживаются
государством.
9.3.3.2. Медико-социальная экспертиза
При проведении восстановительного лечения больных с ПСМТ врач-реабилитолог
должен ориентироваться в вопросах медико-социальной экспертизы.
Сроки временной нетрудоспособности при ПСМТ очень индивидуальны и зависят
от особенностей костных повреждений и степени повреждения спинного мозга, необходимости
повторных оперативных вмешательств, осложнений и т.д. При повреждении костных
структур позвоночника и отсутствии тяжелых повреждений спинного мозга сроки
временной нетрудоспособности определяется в основном стабильностью перелома
В случае стабильного перелома эти сроки чаще ограничиваются 4 месяцами, у лиц
физического труда продлеваются до 8-10 месяцев; в случае нестабильного перелома
временная нетрудоспособность длится до 8-12 месяцев. При отсутствии повреждения
костей позвоночника, но при повреждении спинного мозга сроки временной нетрудоспособности
зависят в первую очередь от перспектив восстановления жизнедеятельности пациента.
При легкой травме спинного мозга временная нетрудоспособность обычно составляет
не менее 1-1.5 месяцев с последующим временным трудоустройством лиц, работа
которых связана с длительной ходьбой, значительным физическим напряжением. При
травме средней степени тяжести сроки временной нетрудоспособности обычно составляют
3-4 месяца, затем в зависимости от прогноза дальнейшего восстановления либо
(при неблагоприятном прогнозе) направляют на БМСЭ для определения группы инвалидности,
либо (при ожидании дальнейшего улучшения, перспективе определить III группу
инвалидности вместо II группы) продлевают временную нетрудоспособность еще на
2-3 месяца. При тяжелой ПСМТ в связи с неблагоприятным клиническим и трудовым
прогнозом продление временной нетрудоспособности свыше 3 месяцев обычно считается
нецелесообразным, больной должен быть освидетельствован в БМСЭ.
Основными причинами ограничения жизнедеятельности и трудоспособности после перенесенной ПСМТ становятся двигательные нарушения (параличи и парезы,
вторичные контрактуры); тазовые нарушения; болевой синдром.
Показаниями для направления больного на БМСЭ с целью определения группы
инвалидности являются [Амелина О.А., 1998]:
- неблагоприятный клинический и трудовой прогноз в связи с выраженным нарушением
функций и социальной жизнедеятельности;
- невозможность вернуться к труду по специальности в связи с имеющимися нарушениями
функций;
- прогрессирующее течение травматической болезни спинного мозга с развитием
поздней функциональной недостаточности, остеохондроза позвоночника с болевым
синдромом.
Критерии инвалидности больных, перенесших ПСМТ [Амелина О.А.,1998]:
I группу инвалидности (резко выраженное ограничение жизнедеятельности)
определяют больным, полностью зависящим от других лиц (неспособность к самостоятельному
передвижению, либо неспособность к самообслуживанию в связи с выраженным нарушением
функций верхних конечностей). После 5 лет наблюдения при неэффективности реабилитационных
мероприятий группа может быть установлена бессрочно.
II группу (выраженное ограничение жизнедеятельности, т.е. способность
к самообслуживанию и передвижению лишь с использованием вспомогательных средств
и/или с помощью других лиц; неспособность к трудовой деятельности либо способность
к трудовой деятельности лишь в специально созданных условиях с использованием
специально оборудованного рабочего места, вспомогательных лиц либо помощи других
лиц) определяют больным с выраженным пара- или гемипарезом, либо умеренным три-
или тетрапарезом; значительными нарушениями тазовых функций; стойким выраженным
болевым синдромом; прогрессирующим течением травматической болезни с развитием
тяжелой посттравматической миелопатии; сложными оскольчатыми и компрессионными
переломами тел позвонков со снижением высоты тел на 1/2 и больше и нестабильностью
в позвоночных сегментах; тяжелой сочетанной травмой; неясным клиническим прогнозом
в случае планируемого оперативного лечения.
III группу инвалидности (умеренное ограничение жизнедеятельности)
определяют больным с умеренными и легкими моно-, пара-, три- и тетрапарезами,
частично ограничивающими возможность передвижения либо выполнения прикладных
действий; больным с умеренным болевым синдромом, умеренными нарушениями тазовых
функций, если эти явления препятствуют работе по основной профессии, либо при
условии снижения квалификации или уменьшении объема производственной деятельности.
Правильное решение вопросов медико-социальной экспертизы важно в первую очередь
для осуществления необходимых мер социальной защиты. В то же время необходимо
понимать, что жесткой связи между необходимой продолжительностью восстановительного
лечения и экспертизой трудоспособности (например, сроками временной нетрудоспособности)
нет. Так, больной, признанный ограниченно трудоспособным, все еще может нуждаться
в восстановительных мероприятиях, которые в этом случае проводятся амбулаторно
во внерабочее время. Определение больному I или II группы инвалидности также
ни в коем случае не означает прекращения реабилитационных мероприятий, если
только к моменту освидетельствования больного на БМСЭ они уже полностью не реализованы.
9.4. ДИФФЕРЕНЦИРОВАННЫЕ ПРОГРАММЫ ВОССТАНОВИТЕЛЬНОГО ЛЕЧЕНИЯ
И КРИТЕРИИ ЭФФЕКТИВНОСТИ РЕАБИЛИТАЦИИ
Прогноз восстановления нарушенных функций при ПСМТ может значительно различаться
в зависимости от степени повреждения спинного мозга и уровня травмы, соответственно
могут существенно различаться цели и задачи медицинской реабилитации. Целесообразно
выделение следующих клинико-реабилитационных групп больных:
I клинико-реабилитационная группа: больные, перенесшие травму позвоночника
с повреждением спинного мозга легкой степени тяжести (сотрясение, ушиб спинного
мозга с незначительными нарушениями его функций);
II клинико-реабилитационная группа: больные, перенесшие среднетяжелую
и тяжелую травму спинного мозга на нижнегрудном и пояснично-крестцовом уровнях;
III клинико-реабилитационная группа: больные, перенесшие среднетяжелую
и тяжелую травму спинного мозга на шейном и верхнегрудном уровнях.
Целью реабилитации больных первой клинико-реабилитационной группы является полное восстановление нормальной жизнедеятельности больного. Задачи
восстановительного лечения: стабилизация поврежденного позвоночно-двигательного
сегмента, устранение (если имеется) деформации позвоночного канала, ликвидация
болевого синдрома, полное восстановление нарушенных в острый период травмы
функций позвоночника и спинного мозга, восстановление социально-бытовой активности
и трудоспособности.
Методы восстановительного лечения включают медикаментозную терапию (анальгетики
при болевом синдроме; препараты, стимулирующие регенерацию костной ткани;
3-х-4-х недельный курс ноотропов и вазоактивных средств); кинезотерапию, направленную
на формирование мышечного корсета и восстановление функциональной полноценности
позвоночника; массаж; при наличии выраженных неврозо- и психопатоподобных
симптомов - психотерапию.
Общий срок восстановительного лечения определяется сроками репаративных процессов
в поврежденных тканях (консолидация губчатой кости, например, наступает в
среднем через 6-8 месяцев). Средняя продолжительность реабилитационного курса
определяется как тяжестью травмы позвоночника, так и степенью поражения спинного
мозга (таблица 9.8).
Критерии эффективности реабилитации: полный регресс болевого синдрома; восстановление
функциональной полноценности позвоночника (восстановление объема безболезненных
движений не менее 60% от нормы и хорошая переносимость вертикальной нагрузки
до 20 кг); восстановление самообслуживания и бытовой активности; для лиц интеллектуального
труда - восстановление трудоспособности, для лиц тяжелого труда - временное
или постоянное трудоустройство.
Целью реабилитации больных второй клинико-реабилитационной группы является достижение максимально возможного уровня независимости пациента в
повседневной жизни. К задачам реабилитации относятся: восстановление самообслуживания,
обучение передвижению без помощи велоколяски; восстановление контролируемых
функций тазовых органов; по возможности - восстановление трудоспособности.
Методы лечения включают курсы указанных в разделах 9.2 и 9.3 медикаментозных
средств и физиотерапевтических процедур, массаж, ИРТ, психотерапию, кинезотерапию,
трудотерапию, восстановление пузырного рефлекса, либо, при сформировавшемся
арефлекторном органическом мочевом пузыре - выполнение пластической заместительной
операции. Для больных с повреждением спинного мозга на пояснично-крестцовом
уровне вполне доступно автомобилевождение. Критерием эффективности этих больных
являются достижение самообслуживания в полном объеме, контролирование функции
тазовых органов, передвижение в фиксирующих аппаратах и с помощью велоколяски,
трудовая деятельность в индивидуальных условиях.
Таблица 9.8. СРЕДНИЕ СРОКИ ВОССТАНОВИТЕЛЬНОГО ЛЕЧЕНИЯ
БОЛЬНЫХ С НЕОСЛОЖНЕННОЙ ТРАВМОЙ ПОЗВОНОЧНИКА И С ЛЕГКИМИ ПОВРЕЖДЕНИЯМИ СПИННОГО
МОЗГА
(по В.И. Соленому, 1994)
Вид травмы |
Характер лечения |
Продолжительность лечения |
Компрессионный стабильный перелом тел позвонков I ст. шейного и грудного
отделов |
консервативное |
до 3-4 месяцев |
| Компрессионный стабильный перелом тел позвонков I ст. поясничного
отдела |
консервативное |
4-6 месяцев |
| Компрессионный стабильный перелом тел позвонков II ст.
шейного и грудного отделов |
консервативное |
4-6 месяцев |
| Компрессионный стабильный перелом тел позвонков II ст. поясничного
отдела |
консервативное |
6-8 месяцев |
| Компрессия III ст. и оскольчатые переломы тел позвонков
шейного отдела |
хирургическое |
до 4 месяцев при исключении физических нагрузок |
| Компрессия III ст. и оскольчатые переломы тел позвонков
грудного отдела |
хирургическое |
до 6 месяцев при исключении физических нагрузок |
| Компрессия III ст. и оскольчатые переломы тел позвонков
грудо-поясничного отдела |
хирургическое |
до 10 месяцев |
| Смещения (нестабильные формы) и вывихи позвонков в шейном
отделе |
вправление открытое (хирургическое) или закрытое смещенных
сегментов |
4-6 месяцев |
| Перелом зуба и дуг второго шейного позвонка |
хирургическое |
6-8 месяцев |
| Нестабильные переломо-вывихи поясничного отдела |
хирургическое |
до 8 месяцев с последующим трудоустройством, лицам физического
труда - определение II группы инвалидности |
| Перелом остистых и/или поперечных отростков от локального
удара |
консервативное |
для лиц интеллектуального труда - 4-5 недель, для лиц физического
труда - 6-8 недель |
| Перелом остистых и/или поперечных отростков от локального
удара в сочетании с разрывом связочного аппарата (флексионно-ротационный
или ротационный механизм травмы) |
консервативное |
для лиц интеллектуального труда - до 2-3 месяцев, для лиц
физического труда - до 3-4 месяцев |
| Сотрясение спинного мозга |
консервативное |
3-4 недели (из них в условиях стационара - не менее 1.5-2
недель) с последующим освобождением от физических нагрузок до 3 месяцев |
| Ушиб спинного мозга без значительных нарушений функций и
без сдавления спинного мозга |
консервативное |
1.5-3 месяца (из них в условиях стационара - не менее 3-4
недель), для лиц физического труда - с последующим трудоустройством |
Целью реабилитации больных самой тяжелой, третьей клинико-реабилитационной
группы является поддержание их жизнеспособности и, по возможности, восстановление
самообслуживания. При уровне повреждения выше С4 поддержание жизнедеятельности
обеспечивается с помощью искусственной вентиляции легких или, при условии
сохранности возбудимости диафрагмального нерва - пейсмекеров этого нерва.
Разработаны компьютеризированные системы, позволяющие больному с тетраплегией
выполнять элементарные действия (открыть дверь, нажать на звонок, перевернуть
страницу и т.д.), либо даже управлять велоколяской с помощью дыхания, голоса,
с помощью движений языка, губ. У многих больных (до 20%) в первые 4 месяца
возникают проблемы с глотанием (в связи с сопутствующей травмой ствола головного
мозга, отеком гортани и глотки после нейрохирургических вмешательства на шейном
уровне, искусственной вентиляции легких [Veis S., Logemann S., 1991]. Прогноз
восстановления функции глотания обычно благоприятный, хотя иногда этот процесс
затягивается на срок до 1 года и требует применения специальной кинезотерапии
для мышц гортани и глотки.
В связи с наличием рефлекторного мочеиспускания больные этой группы требуют
постоянного использования памперсов.
Конкретные возможности восстановления самообслуживания зависят от уровня
поражения. У больных с поражением спинного мозга на уровне С5 сегмента сохранно
сгибание руки в локтевом суставе. Поэтому таких больных реально научить с
помощью специальных ортезов и приспособлений самостоятельно подносить ко рту
ложку, вытирать рот, нажимать кнопки, с посторонней помощью надевать рубашку
или платье. Передвижение возможно с помощью велоколяски с кнопочным управлением.
При поражении на уровне С6 сегмента благодаря сохранности сгибания руки в
локтевом суставе и разгибания кисти больной может научиться самостоятельно
подносить ко рту пищу, умывать и вытирать лицо, надевать одежду на руки и
верхнюю половину туловища. При поражении на уровнях С7-С8 больные дополнительно
приобретают способность самостоятельно поворачиваться в постели, перемещаться
с постели на велоколяску, самостоятельно заменять памперсы, пользоваться велоколяской
с ручным механическим управлением. Больные с поражением на верхнегрудном уровне
выполняют все движения руками и в связи с этим должны стать полностью независимыми
в приеме пищи, выполнении процедур личной гигиены, одевании, передвижении
с помощью велоколяски.
Для этих больных вполне реально переобучение тем видам трудовой деятельности,
которые можно выполнять в положении сидя только с помощью рук (например, ремонт
часов и радиоаппаратуры, работа на компьютере). Продолжительность медицинской
реабилитации больных с повреждением спинного мозга на шейно-грудном уровне
обычно составляет не менее 1.5 лет (так, коррегирующие ортопедические операции
на сухожилиях выполняются в сроки не ранее чем через год после травмы; длительного
времени требует также выработка новых двигательных навыков).
Критерием эффективности реабилитации этих наиболее тяжелых больных с ПСМТ
служит обеспечение хотя бы частичной независимости от окружающих в повседневной
жизни.
ЛИТЕРАТУРА
1. Амелина О.А. Травма спинного мозга // Клиническая неврология с основами
медико-социальной экспертизы: Под ред. А.Ю.Макарова.- СПб.: ООО Золотой век,
1998.- С. 232-248.
2. Антропова М.И.Электростимуляция // Техника и методики физиотерапевтических
процедур: Под ред. В.М.Боголюбова.- М.: Медицина, 1983.
3. Бабиченко Е.И. Классификация позвоночно-спинномозговой травмы / Нейротравматология:
Под ред. А.Н. Коновалова, Л.БЛихтермана, А.А.Потапова.- М.: Вазар-Ферро, 1994.-
С. 252-253.
4. Бабиченко Е.И. Травматическая болезнь спинного мозга / Нейротравматология:
Под ред. А.Н.Коновалова, Л.Б.Лихтерма-на, А.А.Потапова.- М.: Вазар-Ферро,
1994.- С. 292-294.
5. Вейсс М., Зембатый А.Физиотерапия.- М.: Медицина,1986.
6. Вишневский А.А., Лившиц А.В. Электростимуляция мочевого пузыря.- М.: Медицина,
1973.
7. Вогралик В.Г. Основы китайского лечебного метода Чжень-Цзю.- Горький: Горьковское
книжное издательство, 1961.
8. Гайдар Б.В., Шулев Ю.А., Руденко В.В. и др. Реабилитация при позвоночно-спинальной
травме / Медицинская реабилитация: Под ред. Ю.Н.Шанина.- СПб.: Специальная
литература, 1997.- С.496-506.
9. Епифанов В.А. (ред.). Лечебная физическая культура: Справочник.- М.: Медицина,
1987.
10. Коган О.Г. Реабилитация больных при травмах позвоночника и спинного мозга.
- М.: Медицина, 1975.
11. Кривицкая Т.Н. Патоморфология позвоночно-спинномозговой травмы / Нейротравматология:
Под ред. А.Н.Коновалова, Л.Б.Лихтермана, А.А.Потапова.- М.: Вазар-Ферро, 1994-С.
276-277.
12. Кукушкина Т.Н., Докиш Ю.М., Чистякова Н.А. Руководство по реабилитации
больных, частично утративших трудоспособность.- Л.: Медицина, 1981.
13. Лифшиц А.В. Нарушение тазовых функций при позвоночно-спинномозговой травме
/ Нейротравматология: Под ред. А.Н.Коновалова, Л.Б.Лихтермана, А.А.По-тапова.-
М.: Вазар-Ферро, 1994.- С.289-292.
14. Луцик А.А. Повреждения шейного отдела спинного мозга / Нейротравматология:
Под ред. А.Н.Коновалова, Л.Б. Лихтермана, А.А.Потапова.- М.: Вазар-Ферро,
1994.- С. 300-301.
15. Луцик А.А. Оперативное лечение позвоночно-спинномозговой травмы / Нейротравматология:
Под ред. А.Н.Коновалова, Л.Б.Лихтермана, А.А.Потапова.- М.: Вазар-Ферро, 1994.-
С. 265-267.
16. Макаров А.Ю., Амелина О.А. Медико-социальная экспертиза и реабилитация
при травмах спинного мозга: Лекция для слушателей.- Л., 1994.
17. Мачерет Е.Л., Самосюк И.З., Лысенюк В.П. Рефлексотерапия в комплексном
лечении заболеваний нервной системы.- Киев: Здоровья, 1989.
18. Мошков В.Н. Лечебная физическая культура в клинике нервных болезней.-
М.: Медицина, 1982.
19. Меламуд Э.Е. Прогнозирование течения и исходов при позвоночно-спинномозговой
травмы / Нейротравматология: Под ред. А.Н.Коновалова, Л.Б.Лихтермана, А.А.Потапова.-М.:
Вазар-Ферро, 1994.-С. 281.
20. Парфенов А.Я. Отек спинного мозга / Нейротравматология: Под ред. А.Н.Коновалова,
Л.Б. Лихтермана, А.А.Потапова.- М.: Вазар-Ферро, 1994.- С. 272-273.
21. Перльмуттер О.А. Травма позвоночника и спинного мозга.- Н.Новгород, 2000.
22. Потемкин И.М. Уход за больными позвоночно-спинномозговой травмой / Нейротравматология:
Под ред. А.Н.Коновалова, Л.Б.Лихтермана, А-АЛотапова.- М.: Вазар-Ферро, 1994.-
С. 294-295.
23. Правосудов В.П.(ред.). Учебник инструктора по лечебной физической культуре.-
М.: Физкультура и спорт, 1980.
24. Раздольский И.Я. Общие вопросы диагностики травматических повреждений
и заболеваний спинного мозга и позвоночника / Многотомное руководство по хирургии-
М., 1963- Т. 4 - С. 181.
25. Савченко А.Ю. Исходы позвоночно-спинномозговой травмы / Нейротравматология:
Под ред. А.Н.Коновалова, Л.Б.Лихтермана, ААПотапова.- М.: Вазар-Ферро, 1994-С.
250.
26. Соленый В.И. Ортопедические последствия позвоночно-спинномозговой травмы
/ Нейротравматология: Под ред. А.Н.Коновалова, Л.Б.Лихтермана, А.А.Потапова.-
М.: Вазар-Ферро, 1994.- С. 267- 268.
27. Соленый В.И. Врачебно-трудовая экспертиза при позвоночно-спинномозговой
травме / Нейротравматология: Под ред. А.Н.Коновалова, Л.Б.Лихтермана, А.А.Потапова.-
М.: Вазар-Ферро, 1994. - С. 303-304.
28. Сосин И.Н.(ред.). Клиническая физиотерапия: справочник.- Киев: Здоров'я,
1996.
29. Угрюмов В.М., Бабаченко Е.И. Закрытые повреждения позвоночника и спинного
мозга.-М.: Медицина, 1973.
30. Усиков В.Д, Бонохов А.И., Островидова Г.Н. Функциональное лечение в системе
раннего послеоперационного ведения больных с тяжелыми повреждениями позвоночника
/ Проблемы хирургии позвоночника и спинного мозга.- Новосибирск, 1996-С. 60-61.
31. Цивьян Я.Л. Хирургия позвоночника.- Новосибирск, 1993.
32. Чжу Лянь. Руководство по современной Чжень-Цзю терапии.- М.: ГИМЛ, 1959.
33. Шапкин В.И., Бусаков С.С., Одинак М.М. Рефлексотерапия в комплексном лечении
заболеваний и травм нервной системы.- Т.: Медицина, 1987.
34. Ясногородский В.Г. Электродиагностика и электростимуляция / Курортология
и физиотерапия: Под ред. В.М.Боголюбова.- Т. 1.-М.: Медицина, 1985.
35. American Spinal Injury Association: International standarts for neurological
classification of spinal cord injury. Chicago,
American Spinal Injury Association, 1992.
36. Arrowood J.. Mohanty P., Thames M. Cardiovascular problems in the spinal
cord injured patients // Phys.Med. Rehab.-
1987- №1- P. 443-456.
37. Bedbrook G. Spinal injuries with tetraplegia and paraplegia // J. Bone
Joint Surg.Br.- 1979- 1461 - P. 267-284.
38. Brach B., Moser K.,Cedar L. et al. Venous thrombosis in acute spinal cord
paralysis // J.Trauma- 1977 - №17.- P. 289-292.
39. Bracken M., Shepard M., Collins W. et al. Methylprednisolone or naloxone
treatment after acute spinal cord injury: 1 year follow-up data//J.Neurosurg.-
1992.- No 76.- P. 23-31.
40. Carlson S., Parrish M.. Springer J., Doty K., Dosset L. Acute inflammatory
response in spinal cord following impact injury// Exp.Neurol.-1998.- nq 151-
P. 77-88.
41. Chau C., Barbeau H., Rossignol S. Early locomotor training with clonidine
in spinal cats//J.Neurophysiol.- 1998.- №79.-
P. 392-409.
42. Chen H.,Almstrom S.,GimenezLlortL et al. Gait analysis of adult paraplegic
rats after spinal cord repair//Exp.Neurol.- 1997.- №148- P. 544-557.
43. Cosman B., Stone J., Perkash I. The gastrointestinal system/In: Whiteneck
G.G (ed). Aging with spinal cord injury.- New-York: Demos, 1993- P. 117-127.
44. Crozier K., Cheng L.. Graziani V. Et al. Spinal cord injury: prognosis
for ambulation based on quadriceps recovery//Parapдegia.- 1992- № 30- P. 762-767.
45. Denier P., Bregman B. Fetal spinal cord transplants support growth of
supraspinal and segmental growth after spinal cord injury and transplantation
in the adult rat// Exp.Neurol - 1998- hq 149 - P. 13-27.
46. De Vivo M.. Black K.. Stover S. Causes of death during the first 12 years
after spinal cord injury//Arch. Phys. Med. Rehab.- 1993- № 74.- P.248-254.
47. Ditunno J. Predicting recovery after spinal cord injury:a rehabilitation
imperative// Arch.Phys.Med.Rehab-1999 -Vol. 80- №4- P. 361-364.
48. Donovan W., Dimitrijevic M., Dahm L. et al. Neurophysiological approaches
to chronic pain following spinal cord injury//Paraplegia- 1982- hte 20- P.
135-146.
49. Erickson R. Autonomic hyperreflexia: pathophysiology and medical management//
Arch.Phys.Med.Rehab-1980- No 61 - p. 431-440.
50. Feraboli-Lohnherr D., Orsal D., YakovleffA et al. Recovery of locomotor
activity in the adult chronic spinal rat after sublesional transplantation
of embryonic nervous cells: specific role of serotonergic neurones// Exp.Brain
Res.- 1997.- №113.- p. 443-454.
51. Fine P., De Vivo M., McEachran A. Incidence of acute traumatic hospitalized
spinal cord injury in the United States. 1970-1977//Am. J. Epidemiol.- 1982.-
Na 15.- P. 475- 477.
52. FluterG.C. Pulmonary embolism presenting as supraventricular tachycardia
in paraplegia: a case report//Arch. Phys. Med. Rehab- 1993- Iste 74.- P. 1208-1210.
53. Guttman L., Frankel H. The value of intermittent catheterization in the
early management of traumatic paraplegia and tetraplegia //Paraplegia.- 1966.-
No 4.- P. 63"-82.
54. Hall R., Hirsch J., Sackett D. et al. Combined use of leg scanning and
impedance plethysmography in suspected deep venous thrombosis: an alternative
to venography// N.Engl. J.Med.- 1977.- rte 296- P. 1497-1500.
55. Heinemann A.W., Donohue R., Keen M. et al. Alcohol use by persons with
recent spinal cord injury//Arch. Phys. Med. Rehab.- 1988- N9 69.- P. 619-624.
56. Hussey R.W., Stauffer E.S. Spinal cord injury: requirements for ambulation//Arch.
Phys. Med. Rehab.- 1973.- №54.- P. 544-547.
57. Jaeger R.J., Yarkony G.M., Roth E.J. et al. Estimating the user population
of a simple electrical stimulation system for standing // Paraplegia.- 1990.-
№ 28.- P. 505- 511.
58. Johnstone B.R., Jordan C.J., Buntine J.A. A review of surgical rehabilitation
of the upper limb in quadriplegia//Paraplegia.- 1988.- №26- P. 317-339.
59. Kierstead H., Hughes H., Blakemore W. A quantifiable model of axonal regeneration
in the demyelinated adult rat spinal cord//Exp. Neurol- 1998- № 151.- P. 303-313.
60. KelleyM.A., Carson J.L., PalevskyH.I.etal. Diagnosing pulmonary embolism:
new facts and strategies //Ann. Intern. Med.- 1991.- № 114- P. 300-306.
61. Kraus J.F, Franti C.E., Riggins R.S. et al. Incidence of traumatic spinal
cord lesions// J.Chron. Dis- 1975.- Na 28- P. 471- 492.
62. Larson L.F. Overview of disabled drivers' evaluation process//Physical
Disabilities Special Interest Section Newsletter.- 1987-№10-P. 4.
63. Lensing A., Prandoni P., Brandjes D. et al. Detection of deep-vein thrombosis
by real-time B-mode ultrasonography// N.Engl. J.Med- 1989- No 320.- P. 342-345.
64. Lindan R., Joiner E., Freehafer A.A. et al. Incidence and clinical features
of autonomic dysreflexia in patients with spinal cord inju-ries//Paraplegia.-
1980.- № 18.- P. 285-292.
65. Maury M. About pain and its treatment in paraplegics// Paraplegia.-1977.-
No 15.- P. 349-352.
66. Maynard P.M., Glenn G.R., Fountain S.,etal. Neurological prognosis after
traumatic quad-riplegia/AJ.Neurosurg.- 1979.- № 50.- P. 16-24.
67. Merii G. Management of deep vein thrombosis in spinal cord injury//Chest.-
1992.- № 102.- P. 652S-657S.
68. Merii G., Herbison G., Ditunno J. et al. Deep vein thrombosis in acute
spinal cord injured patients//Arch.Phys.Med.Rehab.- 1988.- Na 69- P. 661-664.
69. Merritt J. Management ofspasticity in spinal cord injury//Mayo Clin. Proc.-
1981.- Ns 56- P. 614-622.
70. Mukhin A., Ivanova S., Knoblack S., Faden A. New in vitro model of traumatic
neuronal injury evaluation of secondary injury and glutamate receptor-mediated
neurotoxicity// J.Neu^otrauma.-1997.-№14-P.651- 663.
71. Nixon V. Spinal cord injury: a guide to functional outcomes in physical
therapy management.- Rockville, Md, Aspen,1985.
72. Pierce S. Formula for developing a driving program for the disabled//Physical
Disabilities Special Interest Section Newsletter.- 1987-№10-P. 4.
73. PrivatA., Chauvet N., Gimenez y Ribotta M. Neuronal regeneration and the
glial barrier// Rev. Neurol- 1997.- Na 153.- P. 515- 520.
74. Ramon-CuetoA., Avila J. Olfactory ensheat-ing glia:properties and functions//Brain
Res. Bull- 1998-№46-P. 175-187.
75. Ribotta M., PrivatA. Biological interventions for spinal cord injury//Current
opinion in neurology.- 1999.- Vol 11.- № 6.- P. 647- 652.
76. Rivas D.A., Chancellor M.B., Hill K. et al. Neurological manifestations
of baclofen withdrawal//J.Urol.- 1993.- № 150.- P. 1903-1905.
77. Rossignol S., Dubuc R. Spinal pattern generation//Curr. Opin. Neurol.-
1994.- № 4.- P. 894-902.
78. Stover S.L, Fine P.R. (eds). Spinal Cord Injury: The facts and Figures.-
Birmingham University of Alabama at Birmingham, 1986.
79. Stover S.L., Hataway C.J., Zeiger H.E. He-terotopic ossification in spinal
cord injured patients//Arch.Phys.Med.Rehab.- 1975.- №56-P. 199-204.
80. Stover S.L., Lloyd L.K., Waites K.B. etal. Urinary tract infection in
spinal cord injury//Arch. Phys. Med. Rehab.- 1989.- № 70.- p. 47-54.
81. Stover S.L., Niemann K.M., Miller J.M. Diso-dium etidronate in the prevention
of postoperative reccurence of heterotopic ossification in spinal cord injury
patients/AJ.Bone Joint Surg. Am.- 1976.- Ns 58.- P. 683-688.
82. Stover S.L., Niemann K.M., Tulloss J.R. Experience with surgical resection
of heterotopic bone in spinal cord injury patients//Clin. Prthop- 1991.- №
263.- P. 71-77.
83. Teng Y, Mocchetti I., Wrathall J. Basic and acidic fibroblast growth factors
protect spinal motor neurones in vivo after experimental spinal cord injury//Eur.
J. Neurosci.- 1998.- № 10.- P. 798-802.
84. Trieschmann R.B. (ed). Spinal Cord Injuries: Psychological, Social and
Vocational Adjustment.- Elmsford, N.Y., Pergamon Press, 1976.
85. Vies S.L., Logemann S.A. Dysphagia after spinal cord injury, abstract//ASHA.-1991.-
№33-P. 112.
86. Venier L.H., Ditunno J.F. Heterotopic ossifi cation in the paraplegic
patient//Arch.Phys. Med. Rehab.- 1971.- Ns 52- P. 475- 479.
87. Waring W.P., Karunas R.S. Acute spinal cord injuries and the incidence
of clinically occurring thromboembolic disease//Paraplegia.- 1991-№29-P. 8-16.
88. Waters R.L., Adkins R.H.,Yakura J.S. Definition of complete spinal cord
injury//Para-plegia- 1991.- № 9.- P. 573-581.
89. Waters R.L., Adkins R.H.,Yakura J.S. et al. Motor and sensory recovery
following incomplete paraplegia//Arch. Phys. Med. Rehab- 1994.- Na 75- P.
67-72.
90. Waters R.L., Adkins R.H.,Yakura J.S. et al. Motor and sensory recovery
following complete tetraplegia//Arch. Phys. Med. Rehab.- 1993.- Na 74.- P.
242-247.
91. Waters R.L., Yakura J.S., Adkins R.H.,et al. Determinants of gait performance
following spinal cord injury//Arch.Phys.Med. Rehab.- 1989- Na 70- P. 811-818.
92. Welch R.D., Lobley S.J., O'Sullivan S.B. et al. Functional independence
in quadriplegia:
critical levels//Arch.Phys.Med. Rehab.- 1986- №676- P. .235-240.
93. Yarkony G, Roth E., Cybulski G. Et al. Neu-romuscular stimulation in spinal
cord injury. Prevention of secondary complications// Arch.Phys.Med.Rehab.-
1992.- Na 73- P. 195-200.
94. Yarkony G.,Chen D. Rehabilitation of patients with spinal cord injuries
//In: R.Braddom (ed). Physical medicine and rehabilitation.- W.B.Saunders
Company, 1996.-P. 1149- 1179.
95. Young R., Delwaide P. Drug therapy: spas-ticity//N.Engl. J.Med-1981.-
Na 304.- P. 96-99.
96. Vanek P.,Thallmair M., Schwab M., Kapfham-merJ. Increased lesion-induced
sprouting of corticospinal fibres in the myelin-free rat spinal cord//Eur.
J. Neurosci.- 1998.- Na 10.- P. 45-56.
|
